Glicin
Glicin (skrajšano Gly ali G), je najmanjša od 20 aminokislin, ki jih je običajno srečati v beljakovinah; glicin je tudi najmanjša možna amino kislina - namesto stranske verige kot pri drugih amino kislinah je v glicinu najti en sam vodik. Formula je NH2CH2COOH. Kodoni za glicin so GGU, GGC, GGA, GGG.
Glicin je brezbarvna kristalinična snov sladkega okusa. Med aminokislinami, ki tvorijo proteine, je edinstven, ker je akiralen - njegova zrcalna slika je enaka originalu. Zaradi minimalne stranske verige - enega samega vodikovega atoma - mu ustrezajo tako hidrofilna kot hidrofobna okolja. Acil radikal glicina je glicil.

Zgodovina in etimologija
[uredi | uredi kodo]Glicin so prvič izolirali iz želatine leta 1820.[1] ime izvira iz starogrške besede γλυκύς, to je "sladkega okusa"[2] (kar je tudi izvor predpon glico- in gluco-,na primer v glikoproteinu n in glukozi).
Proizvodnja
[uredi | uredi kodo]Glicin je odkril leta 1820 Henri Braconnot , ko je vzorec želatine prekuhal v žvepleni kislini[3].
Glicin se tvori industrijsko pri obdelavi klorocetne kisline z amoniakom:[4]
- ClCH2COOH + 2 NH3 → H2n ech2COOH + NH4Cl
Po tej poti se letno proizvede 15 milijonov kg te snovi.[5]
V ZDA (GEO Specialty Chemicals, Inc.) in na Japonskem (Showa Denko KK Arhivirano 2014-03-20 na Wayback Machine.) se glicin proizvaja s pomočjo sinteze po Streckerju.[6][7]
V ZDA obstajata dva proizvajalca glicina: Chattem Chemicals, Inc., hčerinsko podjetje Sun Pharmaceutical iz Mumbaja, in podjetje GEO Specialty Chemicals, Inc., ki je odkupilo proizvodne zmogljivosti za glicina in naftalen sulfonat od družbe Hampshire Chemical Corp, hčerinskega podjetja Dow Chemical.[6][8]Proizvodni proces pri Chattem Chemicals (t.i. process "MCA") teče v serijah, končni izdelek vsebuje ostanke klorida, vendar ne sulfata; proizvodnja pri GEO je delno v šaržni obliki, končni izdelek vsebuje nekaj preostalega sulfata, klorida pa ne.
Glicin tudi nastaja kot nečistota v sintezi EDTA med reakcijami so-izdelka amonijaka.[9]
Lastnosti kislina-baza in strukture
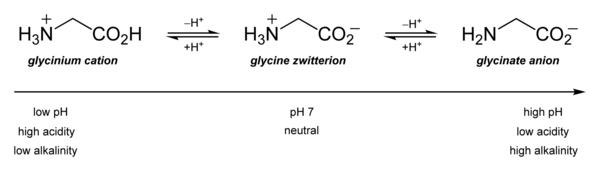
[uredi | uredi kodo]V vodni raztopini je glicin amfoteren: pri nizkih pH se molekula lahko protonira s pKa približno 2.4, pri visokih pH pa izgubi proton s pKa približno 9.6 (natančna vrednost pKa je odvisna od temperature in ionske moči). Naravo glicina v vodni raztopini so raziskovali po teoretični poti.[10] V raztopini je delež koncentracij obeh izomerov neodvisno od analitične koncentracije in od pH. Ta delež je preprosto konstanta ravnotežja za izomerizacijo.
Oba izomera glicina so v plinski fazi dokazali z mikrovalovno spektroskopijo.[11] Strukturo spojine v trdni fazi je podrobno analizirana.[12]
Metabolizem
[uredi | uredi kodo]Biosinteza
[uredi | uredi kodo]Glicin ni bistvenega pomena za človeško prehrano, saj se v telesu sintetizira iz aminokisline serin, ki po drugi strani izvira iz 3-fosfoglicerata, vendar presnovna zmogljivost za bio sintezo glicina ne pokriva potreb pri sintezi kolagena.[13] V večini organizmov encim, serin hidroksimetiltransferaza katalizira pretvorbo s pomočjo kofaktorja piridoksal fosfata:[14]
- serin + tetrahidrofolat → glicin + N5,N10-Metilen tetrahidrofolat + H2O
V jetrih vretenčarjev sintezo glicina katalizira glicin sintetaza (imenovano tudi encim za cepljenje glicina). Ta pretvorba je lahko reverzibilna:[14]
- CO2 + NH4+ + N5,N10-Metilen tetrahidrofolat + NADH + H+ → Glicin + tetrahidrofolat + NAD+
Glicin kodirajo kodoni GGU, GGC, GGA in GGG. Večina beljakovin vsebuje le majhne količine glicina. Pomembna izjema je kolagen, ki vsebuje približno 35 % glicina.[14][15]
Degradacija
[uredi | uredi kodo]Glicin se degradira po treh poteh. Prevladujoča pot v živalih in rastlinah je prek encima za cepljenje glicina:[14]
- Glicin + tetrahidrofolat + NAD+ → CO2 + NH4+ + N5,N10-Metilen tetrahidrofolat + NADH + H+
Glicin je brezbarvna kristalinična snov sladkega okusa. Med aminokislinami, ki tvorijo proteine, je edinstven, ker je ahiralen - njegova zrcalna slika je enaka originalu. Zaradi minimalne stranske verige - enega samega vodikovega atoma - mu ustrezajo tako hidrofilna kot hidrofobna okolja. Acil radikal glicina je glicil.
Po drugi poti se glicin razgradi v dveh korakih. Prvi korak je obrat biosinteze glicina iz serina s pomočjo serin hidroksimetil transferaze. Serin nato encim serin dehidrataza pretvori v piruvat.[14]
Po tretji poti se glicin pretvori v glioksat s pomočjo encima monoaminooksidaza D-amino kislin. Glioksilat nato v jetrih oksidira laktat dehidrogenaza v oksalat v reakciji, ki je odvisna od NAD+.[14]
Razpolovna doba iz glicina in njegovo izločanje iz telesa lahko odvisno od odmerka v veliki meri niha. V eni od raziskav so na primer namerili razpolovni čas med pol ure in štiri ure [16]
Fiziološka funkcija
[uredi | uredi kodo]Glavno vlogo igra glicin kot predhodnik beljakovin, kot je na primer skupaj s hidroksiprolinom v vijačni strukturi kolagena. Predstavlja tudi osnovni gradnik za številne naravne izdelke.
Kot biosintetični intermediat
[uredi | uredi kodo]Glicin je odkril leta 1820 Henri Braconnot, ko je vzorec želatine prekuhal v žvepleni kislini[3].
V višjih evkariontih, je δ-aminolevulinska kislina ključni predhodnik za porfirine; biosintetizira se iz glicina in sukcinil-CoA s pomočjo encima ALA sintetaza. Glicin je vir za vse osrednje podenote C2N purinov.[14]
Kot nevrotransmiter
[uredi | uredi kodo]Glicin zavira nevrotransmiterje v osrednjem živčevju, še posebej v hrbtenici, možganskem deblu in očesni mrežnici. Kadar so receptorji za glicin aktivirani, klorid vstopa v nevron prek ionotropskih receptorjev, kar povzroči inhibitorni postsinaptični potencial (IPSP). Strihnin je močen, bikukulin pa šibek antagonist za ionotropske receptorje glicina, . Glicin je potreben so-agonist, skupaj z glutamatom, za NMDA receptorje.
Pregledni članek o uspavalih iz leta 2014 je opozoril na to, da glicin lahko izboljša kakovost spanja; 3 g glicina pred spanjem je, kot študija navaja, so izboljšali kakovost spanja pri ljudeh.[17][18] Glicin je bil tudi pozitivno preizkušen kot dodatek za zdravljenje shizofrenije.[19]
Uporaba
[uredi | uredi kodo]V ZDA se glicin običajno prodaja v dveh kakovostnih razredih: kot "USP" razred ("United states Pharmacopeia") in kot tehnični razred. Glicin se za različne namene večinoma (80 do 85 odstotkov trga v ZDA) proizvaja s kvalitetno oznako USP.
- Farmacevtska vrsta glicina se proizvaja za nekatere farmacevtske aplikacije, kot intravenozne injekcije, kjer zahteve glede čistosti pogosto presegajo minimalne zahteve za kakovost USP.
- Glicin tehnične čistosti, za katerega ni nujno, da ustreza kakovosti USP, se uporablja v industrijskih aplikacijah; npr. kot agent za kompleksiranje in dokončno obdelavo v kovinski industriji.
Človeška in živalska hrana
[uredi | uredi kodo]Glicin kakovosti USP se med drugim uporablja kot hrani za hišne živali in živalski krmi. Glicin se prodaja kot sladilo/ojačevalec okusa v človeški hrani. Nekatera prehranska dopolnila in beljakovinski napitki vsebujejo glicin.[20] Recepture za nekatera zdravila vsebujejo glicin, ker izboljšuje vpijanje zdravila v želodcu.[20]
Kozmetika in druge uporabe
[uredi | uredi kodo]Glicin služi kot pufer v antacidih, analgetikih, sredstvih proti potenju, kozmetičnih in toaletnih izdelkih.
Glicin je intermediat v sintezi različnih kemičnih proizvodov. Uporablja se v proizvodnji herbicida glifosata.
Laboratorijske raziskave
[uredi | uredi kodo]Glicin, je pomembna sestavina nekaterih raztopin, ki se uporabljajo v analizi beljakovin po metodi SDS-PAGE Kot pufer ohranja pH in preprečuje, da bi med elektroforezo prišlo do poškodbe beljakovin. Z glicinom se tudi odstranjuje protitelesa z membrane za Western blot, kar izboljšuje zaznavanje beljakovin v gelu SDS-PAGE.
Prisotnost v vesolju
[uredi | uredi kodo]Prisotnost glicina v medzvezdnem prostoru je znanstveno potrjena.[21] Leta 2008 so glicin - kot molekulo aminoacetonitrila - sodelavci Instituta Max Planck za Radio Astronomijo odkrili v Large Molecule Heimat, velikem oblaku plina v bližini galaktičnega centra v ozvezdju Strelca.[22] Leta 2009 so potrdili prisotnost glicina v vzorcih, ki jih je vesoljsko plovilo Stardust NASA zajelo s kometa Wild 2. To je prvo odkritje glicina zunaj Zemlje, so pa glicin dokazali tudi v meteoritu Murchison iz leta 1970.[23] Rezultati podpirajo teorijo panspermije, po kateri so gradniki življenja najti po vsem vesolju.[24]
Sklici
[uredi | uredi kodo]- ↑ »glycine«. Encyclopaedia Britannica Online. Pridobljeno 6. decembra 2015.
- ↑ »glycine«. Oxford Dictionaries. Arhivirano iz prvotnega spletišča dne 15. septembra 2016. Pridobljeno 6. decembra 2015.
- ↑ 3,0 3,1 R.H.A. Plimmer (1912) [1908]. R.H.A. Plimmer; F.G. Hopkins (ur.). The chemical composition of the proteins. Monographs on biochemistry. Zv. Part I. Analysis (2 izd.). London: Longmans, Green and Co. str. 82. Pridobljeno 18. januarja 2010.
- ↑ Ingersoll, A. W.; Babcock, S. H. (1932). »Hippuric acid«. Org. Synth. Zv. 12. str. 40.; Coll. Vol., zv. 2, str. 328
- ↑ Karlheinz Drauz, Ian Grayson, Axel Kleemann, Hans-Peter Krimmer, Wolfgang Leuchtenberger, Christoph Weckbecker "Amino Acids" in Ullmann's Encyclopedia of Industrial Chemistry 2007, Wiley-VCH, Weinheim. DOI: 10.1002/14356007.a02_057.pub2
- ↑ 6,0 6,1 »Glycine Conference (prelim)«. USITC. Arhivirano iz prvotnega spletišča dne 27. julija 2011. Pridobljeno 13. junija 2014.
- ↑ [1] Arhivirano 2013-06-13 na Wayback Machine.Wayback Machine.
- ↑ U.S. International Trade Commission, "Glycine From China."
- ↑ Hart, J. Roger (2005) "Ethylenediaminetetraacetic Acid and Related Chelating Agents" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim. DOI: 10.1002/14356007.a10_095
- ↑ Bonaccorsi, R.; Palla, P.; Tomasi, J. (1984). »Conformational energy of glycine in aqueous solutions and relative stability of the zwitterionic and neutral forms. An ab initio study«. J. Amer. Chem. Soc. Zv. 106, št. 7. str. 1945–1950. doi:10.1021/ja00319a008.
- ↑ Suenram, R.D.; Lovas, F.J (1980). »Millimeter wave spectrum of glycine. A new conformer«. J. Amer. Chem. Soc. Zv. 102, št. 24. str. 7180–7184. doi:10.1021/ja00544a002.
- ↑ Jönsson, P.-G.; Kvick, Å (1972). »Precision neutron diffraction structure determination of protein and nucleic acid components. III. The crystal and molecular structure of the amino acid -glycine«. Precision neutron diffraction structure determination of protein and nucleic acid components. III. The crystal and molecular structure of the amino acid -glycine. Zv. B28, št. 6. str. 1827–1833. doi:10.1107/S0567740872005096.
- ↑ »A weak link in metabolism: the metabolic capacity for glycine biosynthesis does not satisfy the need for collagen synthesis«. Journal of biosciences. december 2009. PMID 20093739.
{{navedi revijo}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 14,0 14,1 14,2 14,3 14,4 14,5 14,6 Nelson, David L.; Cox, Michael M. (2005), Principles of Biochemistry (4th ed.
- ↑ Szpak, Paul (2011). »Fish bone chemistry and ultrastructure: implications for taphonomy and stable isotope analysis«. Journal of Archaeological Science. Zv. 38, št. 12. str. 3358–3372. doi:10.1016/j.jas.2011.07.022.
- ↑ Hahn RG (1993). »Dose-dependent half-life of glycine«. Urological Research. Zv. 21, št. 4. str. 289–291. doi:10.1007/BF00307714. PMID 8212419.
- ↑ Halson SL (2014). »Sleep in elite athletes and nutritional interventions to enhance sleep«. Sports Med. Zv. 44 Suppl 1. str. S13–23. doi:10.1007/s40279-014-0147-0. PMC 4008810. PMID 24791913.
- ↑ Yamadera W; Inagawa K; Chiba S; Bannai M; Takahashi M; Nakayama K (2007). »Glycine ingestion improves subjective sleep quality in human volunteers, correlating with polysomnographic changes«. Sleep and Biological rhythms. Zv. 5, št. 2. str. 126–131. doi:10.1111/j.1479-8425.2007.00262.x.
- ↑ Coyle JT; G Tsai (2004). »The NMDA receptor glycine modulatory site: a therapeutic target for improving cognition and reducing negative symptoms in schizophrenia«. Psychopharmacology. Zv. 174. str. 32–28. doi:10.1007/s00213-003-1709-2.
- ↑ 20,0 20,1 [2][mrtva povezava]
- ↑ Snyder LE; Lovas FJ; Hollis JM; in sod. (2005). »A rigorous attempt to verify interstellar glycine«. Astrophys J. Zv. 619, št. 2. str. 914–930. arXiv:astro-ph/0410335. Bibcode:2005ApJ...619..914S. doi:10.1086/426677.
- ↑ Staff. »Organic Molecule, Amino Acid-Like, Found In Constellation Sagittarius 27 March 2008 - Science Daily«. Pridobljeno 16. septembra 2008.
- ↑ Kvenvolden, Keith A.; Lawless, James; Pering, Katherine; Peterson, Etta; Flores, Jose; Ponnamperuma, Cyril; Kaplan, Isaac R.; Moore, Carleton (1970). »Evidence for extraterrestrial amino-acids and hydrocarbons in the Murchison meteorite«. [[|Nature]]. Zv. 228, št. 5275. str. 923–926. Bibcode:1970Natur.228..923K. doi:10.1038/228923a0. PMID 5482102.
- ↑ »Building block of life found on comet«. Reuters. 18. avgust 2009. Pridobljeno 18. avgusta 2009.

![{\displaystyle K=\mathrm {\frac {[H_{3}N^{+}CH_{2}CO_{2}^{-}]}{[H_{2}NCH_{2}CO_{2}H]}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/80281edf6f4791a13bbe2bd60977ae8cb2e970e0)