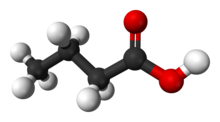
Butanojska kislina
| |||
| |||
| Imena | |||
|---|---|---|---|
| IUPAC ime
butanojska kislina
| |||
| Druga imena
propankarboksilna kislina
| |||
| Identifikatorji | |||
3D model (JSmol)
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.003.212 | ||
| EC število |
| ||
| KEGG | |||
| MeSH | Butyric+acid | ||
PubChem CID
|
|||
| RTECS število |
| ||
| UNII | |||
| UN število | 2820 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Lastnosti | |||
| C4H8O2 | |||
| Molska masa | 88,11 g·mol−1 | ||
| Videz | brezbarvna tekočina | ||
| Vonj | neprijeten | ||
| Gostota | 1,135 g/cm3 (−43 °C)[1] 0,9528 g/cm3 (25 °C)[2] | ||
| Tališče | −5,1 °C (22,8 °F; 268,0 K) | ||
| Vrelišče | 163,75 °C (326,75 °F; 436,90 K) | ||
| Sublimacijske okoliščine | pri −35 °C sublimira ΔsublH | ||
| z vodo se meša v vseh razmerjih | |||
| Topnost | rahlo topna v ogljikovem tetrakloridu,[4] meša se z etanolom in etrom | ||
| log P | 0,79[4] | ||
| Parni tlak | 0,112 kPa (20 °C)[5] 0,74 kPa (50 °C) 9,62 kPa (100 °C)[4] | ||
| kH | 5,35,10-4 L·atm/mol[4] | ||
| Kislost (pKa) | 4,82[4] | ||
| Toplotna prevodnost | 1,46·105 W/m·K | ||
| Lomni količnik (nD) | 1,398 (20 °C)[2] | ||
| Viskoznost | 1,814 cP (15 °C)[6] 0,1426 cP (25 °C)[4] | ||
| Struktura | |||
| Kristalna struktura | monoklinska (−43 °C)[4] | ||
| Prostorska skupina | C2/m[4] | ||
a = 8,01, b = 6,82, c = 10,14[4] α = 90°, β = 111,45°, γ = 90°
| |||
| Dipolni moment | 0,93 D (20 °C)[6] | ||
| Termokemija | |||
| Specifična toplota, C | 178,6 J/mol·K[3][4] | ||
| Standardna molarna entropija S |
222,2 J/mol·K[3] | ||
Std tvorbena
entalpija (ΔfH⦵298) |
−533,9 kJ/mol | ||
Std sežigna
entalpija (ΔcH⦵298) |
2183,5 kJ/mol[3] | ||
| Nevarnosti | |||
| GHS piktogrami |  [7] [7]
| ||
| Opozorilna beseda | Nevarno | ||
| H314[7] | |||
| P280, P305+351+338, P310[7] | |||
| NFPA 704 (diamant ognja) | |||
| Plamenišče | 71 do 72 °C (160 do 162 °F; 344 do 345 K) | ||
| 440 °C (824 °F; 713 K) | |||
| Meje eksplozivnosti |
2,2–13,4% | ||
| Smrtni odmerek ali koncentracija (LD, LC): | |||
LD50 (srednji odmerek)
|
2000 mg/kg (oralno, podgana) | ||
| Sorodne snovi | |||
| Sorodno karboksilne kisline | propanojska kislina akrilna kislina jantarna kislina jabolčna kislina vinska kislina krotonska kislina fumarska kislina pentanojska kislina | ||
| Sorodne snovi | 1-butanol butiraldehid metil butirat | ||
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |||
| Sklici infopolja | |||
Masléna kislína (iz grškega βούτῡρον [butiron] - maslo, IUPAC-ime: butanojska kislina) je karboksilna kislina s kemijsko formulo CH3CH2CH2-COOH. Nahaja se med drugim v žaltavem maslu, po čemer je dobila ime. Maslena kislina je tudi v parmezanu in izbljuvkih in daje značilen telesni vonj.
Soli in estri maslene kisline se imenujemo butanoati ali butirati.
Maslena kislina ima žarek okus s sladkastim priokusom in neprijeten vonj. Človek lahko zazna koncentracijo 10 ppm, medtem ko lahko nekateri sesalci zaznajo veliko manjše količine, na primer pes 10 ppb.
Kemijske lastnosti
[uredi | uredi kodo]Maslena kislina je kratkoverižna maščobna kislina, ki se pojavlja v naravnih maščobah in oljih zlasti v obliki estrov. Trigliceridi z masleno kislino predstavljajo okoli 3–4 % masla. Ko maslo postane žaltavo, se maslena kislina zaradi hidrolize sprosti iz trigliceridov in zaznamo neprijeten vonj. Je šibka kislina z vrednostjo pKa 4,82 (podobno kot ocetna kislina, pri kateri je pKa 4,76).[8] Maslena kislina se v čisti obliki nahaja pri sobnih razmerah v obliki brezbarvne kapljevine, ki se zlahka meša z vodo, etanolom in etrom. Od vodne faze jo lahko ločimo z dodatkom soli, na primer kalcijevega klorida.
Strukturni izomer maslene kisline je izomaslena ali 2-metilpropanojska kislina.
Pridobivanje
[uredi | uredi kodo]Industrijsko jo pridobivajo s fermentacijo sladkorja ali škroba ob dodatku pokvarjenega sira; dodan kalcijev karbonat nevtralizira nastale kisline. Fermentacija škroba do maslene kisline pospeši bakterija Bacillus subtilis.
sklici
[uredi | uredi kodo]- ↑ F.J. Strieter, D.H. Templeton (1962). Crystal structure of butyric acid. Acta Crystallographica 15 (12): 1240. doi: 10.1107/S0365110X6200328X.
- ↑ 2,0 2,1 2,2 2,3 D.R. Lide, urednik (2009). CRC Handbook of Chemistry and Physics. 90. Izdaja. Boca Raton, Florida: CRC Press. ISBN 978-1-4200-9084-0.
- ↑ 3,0 3,1 3,2 3,3 P.J. Lindstrom, W.G. Mallard, urednika. Butanoic acid. NIST Chemistry WebBook. NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD. Pridobljeno 13. Junija 2014.
- ↑ 4,00 4,01 4,02 4,03 4,04 4,05 4,06 4,07 4,08 4,09 Butyric acid. PubChem.
- ↑ Butanoic Acid. ALS Environmental. Pridobljeno 13. junija 2014.
- ↑ 6,0 6,1 Butanoic acid Arhivirano 2016-05-09 na Wayback Machine..
- ↑ 7,0 7,1 7,2 Sigma-Aldrich Co., Butyric acid. Pridobljeno 2014-06-13.
- ↑ »Adimix Sodium Butanoate information« (PDF). Arhivirano (PDF) iz spletišča dne 26. marca 2009. Pridobljeno 27. oktobra 2008.



