Epilepsija
| Epilepsija | |
|---|---|
 | |
| Elektroencefalogram epileptičnega napada | |
| Specialnost | nevrologija |
| Simptomi | epizode izgube zavesti, nenormalnega tresenja, strmenja, spremembe vida, sprememb razpoloženja in/ali drugih kognitivnih motenj[1] |
| Trajanje | kronično |
| Vzroki | neznan vzrok, poškodba možganov, kap, možganski tumorji, okužbe možganov, prirojene okvare[1][2][3] |
| Diagnostični postopki | elektroencefalografija, izključitev drugih možnih vzrokov[4] |
| Zdravljenje | zdravila, operacija, nevrostimulacija, sprememba prehrane[5][6] |
| Prognoza | obvladljiva v 69 %[7] |
| Pogostost | 51,7 mio./0,68 % (2021)[8] |
| Smrti | ~140 000 (2021)[9] |
| Klasifikacija in zunanji viri | |
| MKB-10 | G40–G41 |
| MKB-9 | 345 |
| DiseasesDB | 4366 |
| MedlinePlus | 000694 |
| eMedicine | neuro/415 |
| MeSH | D004827 |
Epilepsíja (iz starogrškega glagola ἐπιλαμβάνειν, to je »zgrabiti, posedovati ali mučiti«),[10] ljudsko božjást ali pádavica,[11] je skupina kroničnih nevroloških motenj, za katere so značilni ponavljajoči se epileptični napadi.[12] Napadi lahko variirajo od zelo kratkih in skoraj neopaznih do dolgih obdobij zelo močnega tresenja.[1] Povzročijo lahko poškodbe, bodisi neposredno, na primer zlome kosti zaradi padca, bodisi posredno, če oseba zaradi napada povzroči nesrečo.[1] Epileptični napadi se po navadi ponavljajo in nimajo nekega osnovnega vzroka,[13] medtem ko posamezni napadi, ki se pojavijo zaradi posebnega vzroka, ne veljajo za epileptične.[14]
Mehanizem, ki povzroči epileptični napad, so nenormalne, prekomerne in usklajene razelektritve živčnih celic v možganski skorji,[14] kar je mogoče zaznati na elektroencefalogramu. Razlog za ta pojav je pri večini primerov epilepsije neznan,[1] nekateri primeri pa se razvijejo kot posledica poškodbe možganov, kapi, možganskega tumorja, okužbe možganov ali prirojene okvare (epileptogeneza).[1] Majhen delež primerov neposredno povezujejo z znanimi genskimi mutacijami.[4][15] Pri diagnozi se poskuša izločiti morebitne druge dejavnike, ki bi lahko povzročili podobne simptome (kot je sinkopa), in ugotoviti, ali je bil prisoten kateri od drugih možnih vzrokov za napade (na primer odtegnitev alkohola ali težave z elektroliti).[4] To se stori med drugim s slikanjem možganov in s preiskavo krvi.[4] Epilepsija se lahko pogosto potrdi z elektroencefalografijo, vendar pa normalen elektroencefalogram ne pomeni, da je epilepsija izključena.[4]
Epilepsijo, ki se pojavi kot posledica drugih težav, je mogoče preprečiti.[1] V približno 70 % primerov se napadi lahko nadzorujejo z zdravili.[7] Pri ljudeh, katerih napadi se na zdravila ne odzivajo, lahko v poštev pride operacija, nevrostimulacija ali sprememba prehranjevalnih navad.[5][6] Niso vsi sindromi epilepsije vseživljenjski in precejšno število ljudi izboljša svoje stanje do točke, na kateri zdravila niso več potrebna.[1]
Epilepsijo ima okoli 10.000 ljudi v Sloveniji[16] in okoli 51 milijonov ljudi na svetu.[17] Skoraj 80 % primerov se pojavlja v državah v razvoju.[18] Epilepsija je pogostejša pri otrocih in starejših osebah.[19][20] V razvitem svetu se novi primeri najpogosteje pojavljajo pri dojenčkih in starejših osebah;[21] v deželah v razvoju pa pri starejših otrocih in mlajših odraslih osebah[22] zaradi razlik v pogostosti temeljnih vzrokov. Okoli 5 do 10 % celotne populacije bo doživelo obliko neizzvanega napada do starosti 80 let,[23] verjetnost, da bodo manj kot dve leti po prvem utrpeli še en napad, pa je okoli 40 %.[24][25] V mnogih predelih sveta je osebam z epilepsijo omejeno ali prepovedano voziti, vendar večina spet lahko vozi po določenem času brez napadov.[26]
Znaki in simptomi
[uredi | uredi kodo]
Za epilepsijo je značilno dolgotrajno tveganje ponavljajočih se napadov.[27] Ti napadi se lahko prikažejo na več načinov, glede na to, kateri del možganov je vključen, in glede na starost osebe.[27][28]
Napadi
[uredi | uredi kodo]Najpogostejša vrsta (60 %) napadov so konvulzivni napadi z neobvladljivim krčenjem mišic.[28] Od tega se jih tretjina začne kot generaliziran napad, ki prizadene obe možganski polobli in zavest, dve tretjini napadov pa se začneta kot žariščni napad (v eni izmed polobel), ki potem lahko napredujejo v generalizirane napade.[28] Preostalih 40 % napadov je nekonvulzivnih. Primer te vrste je odsotnostni napad, ki se kaže kot zmanjšana raven zavesti in po navadi traja okoli 10 sekund.[2][29]
Pred žariščnim napadom pride pogosto do določenih doživetij, ki so znani kot avra.[30] Med drugim gre za čutilne (vidne, slušne ali vonjalne) doživljaje ter psihične, avtonomne ali motorične fenomene, odvisno od vpletenega predela možganov.[2] Trzljaji se lahko začnejo v določeni skupini mišic in se nato razširijo na okoliške; tak pojav je znan kot jacksonski napad.[31] Lahko pride do avtomatizmov; gre za nezavedne dejavnosti, ki so večinoma enostavni, ponavljajoči se gibi, kot je cmokanje, ali pa gre za bolj zapletene gibe, kot je pobiranje kake stvari s tal.[31]
Generaliziranih napadov obstaja šest vrst: tonično-klonični, tonični, klonični, mioklonični, odsotnostni in atonični napadi.[32] Pri vseh pride do izgube zavesti in se praviloma pripetijo brez opozorila.
Tonično-klonični napadi se javijo s krčenjem okončin, ki jih prizadeti nato iztegne, hrbet pa se mu usloči; to traja 10–30 sekund (tonična faza).Zaradi skrčenja prsnih mišic je lahko slišati krik. Temu potem sledi usklajeno tresenje okončin (klonična faza). Pri toničnem napadu pride do neprenehnega krčenja mišic. Prizadeti pogosto pomodri, ker preneha dihati. Pri kloničnem napadu je tresenje okončin usklajeno. Ko se tresenje ustavi, lahko traja še 10–30 minut, dokler se oseba ne povrne v normalno stanje; to obdobje imenujemo »postiktalna faza«. Med napadom lahko pride do izgube nadzora nad črevesjem ali mehurjem.[18] Oseba se lahko ugrizne v vrh ali rob jezika.[33] Pri tonično-kloničnem napadu so pogostejši ugrizi ob straneh.[33] Ugrizi v jezik so razmeroma pogosti tudi pri psihogenih neepileptičnih napadih – napadih, ki jih ne spremlja usklajena razelektritev, vidna na EEG, in se štejejo za disociativno motnjo.[33]
Med miotoničnimi napadi pride do zelo kratkih mišičnih krčev samo na nekaterih območjih ali pa povsod.[34][35] Zaradi takšnega napada lahko prizadeta oseba pade in se poškoduje.[34] Odsotnostni napadi so lahko blagi, s komaj zaznavnim obratom glave ali mežikanjem z očmi;[2] oseba se ne prevrne in se vrne v normalno stanje, takoj ko se napad konča.[2] Atonični napadi pomenijo izgubo mišične dejavnosti za dlje kot eno sekundo,[31] po navadi na obeh straneh telesa.[31] Redkejši tipi napadov lahko povzročijo neobvladljiv nenaraven smeh (gelastični), jok (diskrastični) ali zapletenejša doživetja, na primer déjà vu.[35]
Okoli 6 % oseb z epilepsijo ima napade, ki jih pogosto sprožijo posebni dogodki, in so znani kot refleksni napadi.[36] Napade pri osebah z refleksno epilepsijo sprožijo samo določeni, posebni dražljaji.[37] Pogosti sprožilci so na primer utripajoče luči in nenadni zvoki.[36] Pri nekaterih vrstah epilepsije se napadi pojavljajo pogosteje med spanjem,[38] pri nekaterih vrstah pa skoraj izključno tedaj.[39] Leta 2017 je Mednarodna liga proti epilepsiji objavila nove enotne smernice za klasifikacijo napadov in epilepsij skupaj z njihovimi vzroki in pridruženimi težavami.[40]
Roji napadov
[uredi | uredi kodo]Ljudje z epilepsijo lahko doživijo roje napadov, ki se jih lahko v grobem definira kot akutno poslabšanje nadzora nad napadi.[41] Pojavnost rojev napadov ni natančno znana predvsem zaradi različnih definicij, uporabljenih v različnih raziskavah,[42] ocenjuje pa se, da se pojavlja pri 5 do 50 % oseb z epilepsijo.[43] Največje tveganje za pojav roja napadov imajo ljudje z odporno epilepsijo in visoko pogostostjo napadov.[44][45][46] Roji napadov povzročajo večjo obremenitev zdravstva, slabšo kakovost življenja, moteno psihosocialno funkcioniranje in verjetno višjo smrtnost.[42][47] Za akutno zdravljenje rojev napadov se uporabljajo benzodiazepini.[48]
Postiktalno obdobje
[uredi | uredi kodo]Ko je aktivnega napada (iktalnega obdobja) konec in preden se vrne normalna raven zavesti, običajno nastopi tako imenovano postiktalno obdobje, to je obdobje zmedenosti.[30] Po navadi traja od 3 do 15 minut,[49] lahko pa tudi več ur.[50] Drugi pogosti simptomi so utrujenost, glavobol, težave pri govoru in nenormalno vedenje.[50] Psihoza po napadu je dokaj pogosta in se pojavi pri 6–10 % ljudi.[51] Ljudje se pogosto ne spomnijo, kaj se je v tem času zgodilo.[50] Po žariščnem napadu se lahko tudi pojavi lokalizirana onemoglost, znana kot Toddova paraliza. Če se pojavi, traja po navadi od nekaj sekund do nekaj minut, v redkih primerih pa lahko traja dan ali dva.[52]
Psihosocialni vidiki
[uredi | uredi kodo]Epilepsija lahko škodljivo učinkuje na družbeno in psihološko dobro počutje.[28] Ti učinki so lahko med drugim družbena osamitev, stigmatizacija ali invalidnost.[28] Lahko so vzrok za nižje uspehe v izobraževanju in za slabše možnosti zaposlitve.[28] Pri ljudeh z epilepsijo, zlasti otrocih, so pogoste učne težave.[28] Stigmo epilepsije lahko občuti tudi družina obolelega.[18]Pri ljudeh z epilepsijo se, delno odvisno od epileptičnega sindroma, pogosteje pojavljajo nekatere motnje, med njimi depresija, anksioznost, obsesivno-kompulzivna motnja[53] in migrena.[54] Motnja pozornosti s hiperaktivnostjo (ADHD) prizadene tri- do petkrat več otrok z epilepsijo kot otrok brez nje.[55] ADHD in epilepsija močno vplivata na otrokov vedenjski, učni in socialni razvoj.[56] Epilepsija je pogostejša tudi pri otrocih z avtizmom.[57]
Približno vsaka tretja oseba z epilepsijo ima vseživljenjsko zgodovino duševne motnje.[58] Temu se pripisuje več razlogov, vključno s patofiziološkimi spremembami, povezanimi s samo epilepsijo, in tudi negativnim izkušnjam, do katerih je življenje z epilepsijo privedlo (npr. stigmi, diskriminaciji).[59] Poleg tega se domneva, da povezava med epilepsijo in duševnimi motnjami ni enostranska, marveč dvosmerna: na primer, pri ljudeh z depresijo obstaja večje tveganje za razvoj novonastale epilepsije.[60]
Sopojavnost depresije ali anksioznosti z epilepsijo se povezuje s slabšo kakovostjo življenja, večjo smrtnostjo, večjo obremenitvijo zdravstva in slabšim odzivanjem na zdravljenje (tudi kirurško).[61][62][63][64] Z anksioznimi motnjami in depresijo je mogoče razložiti več variabilnosti v kakovosti življenja kot z vrsto ali pogostostjo napadov.[65] Obstajajo dokazi, da tako depresija kot anksiozne motnje pri ljudeh z epilepsijo niso dovolj pogosto diagnosticirane niti zdravljene.[66]
Vzroki
[uredi | uredi kodo]Vzroki za epilepsijo so lahko tako genetski kot pridobljeni, pogosto pa kombinacija obojih.[67][68] Znani neprirojeni vzroki so med drugim huda možganska poškodba, kap, tumorji in težave z možgani zaradi predhodne okužbe.[67] V okoli 60 % primerov vzrok ni znan.[18][28] Epilepsije zaradi genetskih, prirojenih in razvojnih motenj so pogostejše med mlajšimi ljudmi, možganski tumorji in kapi pa so pogostejši vzroki pri starejših.[28]
Napadi se lahko pojavijo tudi kot posledica drugih zdravstvenih težav;[32] če se pojavijo precej blizu določenega vzroka, kot je kap, poškodba glave, zaužitje strupene snovi ali presnovna težava, se imenujejo akutni simptomatični napadi in se uvrščajo v širšo klasifikacijo motenj, povezanih z napadi, ne pa pod samo epilepsijo.[17][69]
Genetika
[uredi | uredi kodo]Genetika naj bi bila neposredno ali posredno povezana z večino primerov.[15][70] Nekatere epilepsije se razvijejo zaradi okvare enega gena (1–2 %), večina pa zaradi interakcije več genov in okoljskih dejavnikov.[15] Vsaka monogenska okvara je redka, vseh opisanih pa je prek 200.[71] Večina udeleženih genov vpliva neposredno ali posredno na ionske kanalčke.[67] To vključuje gene za ionske kanalčke, encime, receptorje GABA in s proteinom G sklopljene receptorje.[34]
Če ima epilepsijo eden od enojajčnih dvojčkov, obstaja 50–60-% verjetnost, da jo bo imel tudi drugi.[15] Pri dvojajčnih dvojčkih je ta verjetnost 15-%.[15] Tveganje je večje pri tistih z generaliziranimi napadi kot pri tistih z žariščnimi.[15] Če za epilepsijo trpita oba dvojčka, imata večinoma isti epileptični sindrom (70–90 %).[15] Za druge bližnje sorodnike je tveganje petkrat večje kot pri splošni populaciji.[72] Epilepsijo ima med 1 in 10 % oseb z Downovim sindromom in 90 % oseb z Angelmanovim sindromom.[72]
Fakomatoze
[uredi | uredi kodo]Fakomatoze, znane tudi kot nevrokutane motnje, so skupina večsistemskih bolezni, ki najmočneje prizadenejo kožo in osrednji živčni sistem. So posledica nepravilnega razvoja zarodkovega ektodermalnega tkiva, ki ga najpogosteje povzroči mutacija enega gena. Ker se iz ektoderma razvijejo možgani in ostalo živčno tkivo ter koža, lahko okrnjen razvoj povzroči epilepsijo, pa tudi avtizem, duševni primanjkljaj in druga stanja. Pri nekaterih tipih fakomatoz, na primer tuberozni sklerozi in Sturge-Weberjevem sindromu, je pogostost epilepsije večja kot pri drugih, na primer nevrofibromatozi tipa 1.[73]
Tuberozna skleroza nastane zaradi mutacij v genu TSC1 ali TSC2, deduje se avtosomalno dominantno in prizadene približno enega na 6000–10 000 živorojenih otrok.[74][75] Mutacije povzročijo prekomerno aktivnost signalne poti mTOR (mehanistična tarča rapamicina), kar vodi v tvorbo tumorjev v različnih organih, na primer možganih, koži, srcu, očeh in ledvicah.[75] Poleg tega naj bi nenormalno delovanje mTOR povzročalo spremembe vzdražljivosti živčnih celic.[76] Prevalenca epilepsije se ocenjuje na 80–90 %.[73][76] Večina primerov epilepsije se izrazi v prvih treh letih življenja in se ne odzivajo na zdravila.[77] Sorazmerno nove možnosti za obvladovanje epilepsije pri osebah s tuberozno sklerozo so inhibitorji mTOR, kanabidiol in vigabatrin. Pogosta je odločitev za kirurški poseg.
Sturge-Weberjev sindrom povzroča mutacija gena GNAQ in je prisotna pri enem na 20 000–50 000 živorojenih otrok.[78] Zaradi mutacije pride do žilnih malformacij, ki prizadenejo možgane, kožo in oči. Običajno se to izrazi v madežu rdečega vina podobnem znamenju na obrazu, očesnih angiomih in možganskih žilnih malformacijah, ki so najpogosteje prisotni na eni strani, v 15 % primerov pa na obeh.[79] Prevalenca epilepsije je 75–100-% in višja pri osebah s prizadetima obema polovicama.[79] Napadi se običajno zgodijo v prvih dveh letih življenja in so v slabi polovici primerov odporni na zdravila.[80] Uspešneje, po nekaterih podatkih v celo 83 %, napade odpravi kirurški poseg.[81]
Nevrofibromatoza tipa 1 je najpogostejša fakomatoza, ki se pojavi pri približno enem na 3000 živorojenih.[82] Povzroča jo avtosomalna dominantna mutacija na genu za nevrofibromin 1. Stanje se izraža različno, povzroči pa lahko hiperpigmentacije na koži, hamartome na šarenici (Lischeve nodule), nevrofibrome, gliome na optični poti in kognitivno prizadetost. Prevalenca epilepsije je ocenjena na 4–7 %.[83] Napade je v primerjavi z drugimi fakomatozami sorazmerno lahko nadzorovati z zdravili, če temu ni tako, pa v poštev pride kirurški poseg.[84]
Drugo
[uredi | uredi kodo]Epilepsija se lahko pojavi kot posledica številnih drugih stanj, na primer tumorjev, kapi, poškodb glave, predhodnih okužb osrednjega živčevja, genetskih motenj in možganskih poškodb ob rojstvu.[18][32] Skoraj 30 % oseb z možganskimi tumorji ima epilepsijo, zato so ti vzrok za približno 4 % primerov.[72] Tveganje je največje pri tumorjih v senčnem režnju in pri tistih, ki rastejo počasi.[72] Pri drugih večjih lezijah, kot so cerebralne kavernozne skaženosti in artiovenske skaženosti, je tveganje kar 40–60-odstotno.[72] Epilepsija se razvije pri 2–4 % oseb, ki jih je zadela kap.[85][86] Dejavniki tveganja za epilepsijo po kapi so resnost kapi, vključenost korteksa, krvavitve in predhodni napadi.[87][88] Med 6 in 20 % primerov epilepsije se pripisuje travmam glave.[72] Lažje možganske poškodbe tveganje povečajo za približno dvakrat, hujše možganske poškodbe pa za sedemkrat.[72] Pri tistih, ki so preživeli močan strel v glavo, je tveganje približno 50-odstotno.[72]
Nekateri izsledki povezujejo epilepsijo s celiakijo in neceliakalno občutljivostjo na gluten, medtem ko drugi te povezave ne podpirajo. Zdi se, da obstaja sindrom, ki se izraža s celiakijo, epilepsijo in kalcifikacijami v možganih.[89][90] Pregled iz leta 2012 ocenjuje, da ima med 1 in 6 % epileptikov celiakijo, medtem ko je v splošni populaciji njena pogostost 1-%.[90]
Tveganje za epilepsijo po meningitisu je manj kot 10-odstotno, pogosteje pa ta bolezen povzroča napade med samo okužbo.[72] Pri herpetičnem encefalitisu je nevarnost napada okoli 50-odstotna[72] z visokim tveganjem za poznejšo epilepsijo (do 25-odstotnim).[91][92] Oblika okužbe s prašičjo trakuljo (cisticerkoze), ki prizadene možgane (nevrocisticerkoza), je vzrok za do polovico primerov epilepsije v predelih sveta, kjer je ta zajedavec razširjen.[72] Epilepsija se lahko pojavi tudi po drugih možganskih okužbah, kot so cerebralna malarija, toksoplazmoza in toksokariaza.[72] Dolgotrajno prekomerno uživanje alkohola poveča nevarnost za epilepsijo: tisti, ki popijejo šest enot alkohola na dan, so dvainpolkrat bolj izpostavljeni nevarnosti.[72] Med druga tveganja spadajo Alzheimerjeva bolezen, multipla skleroza in avtoimuni encefalitis.[72] Cepljenje ne povečuje tveganja za epilepsijo.[72] Nedohranjenost je dejavnik tveganja, prisoten večinoma v državah v razvoju, ni pa jasno, ali gre za neposredni vzrok ali se oboje zgolj pojavlja na istih območjih.[22] Tveganje epilepsije je večje pri ljudeh s cerebralno paralizo: ima jo polovica ljudi s spastično kvadriplegijo in s spastično hemiplegijo.[93]
Mehanizem
[uredi | uredi kodo]Navadno je možganska električna dejavnost nesinhrona, saj se istočasno ne proži veliko število živčnih celic, marveč se celice prožijo po vrsti, kot signali potujejo po možganih.[2] Dejavnost nevronov nadzorujejo različni dejavniki, tako znotrajcelični kot v njihovi okolici. Znotrajnevronski dejavniki so med drugim vrsta, število in razporeditev ionskih kanalčkov, spremembe receptorjev in spremembe izražanja genov.[94] Dejavniki v okolici nevrona zajemajo koncentracije ionov, sinaptično plastičnost in uravnavanje razgradnje prenašalcev s strani glia-celic.[94][95]
Epilepsija
[uredi | uredi kodo]Natančen mehanizem epilepsije ni poznan,[96] nekaj pa je znanega o njenih celičnih in omrežnih mehanizmih. Kljub temu ni znano, katere okoliščine v možganih sprožijo napad s prekomerno sinhronizacijo.[97][98][99][100]
Potem ko se ekscitatorni nevron sproži, običajno za nekaj časa postane odpornejši na proženje, deloma zaradi vpliva zaviralnih (inhibitornih) nevronov, električnih sprememb v ekscitatornem nevronu in negativnih vplivov adenozina.[2] Pri epilepsiji je odpornost ekscitatornih nevronov na vnovično vzdraženje zmanjšana.[2] Razlog za to so lahko spremembe v ionskih kanalčkih ali nepravilno delovanje zaviralnih nevronov.[2] Posledično nastane območje, znano kot »žarišče«, kjer se lahko razvijejo napadi.[2] Drugi mehanizem epilepsije bi lahko bil nadregulacija ekscitatornega ali podregulacija zaviralnega živčevja po poškodbi možganov.[2][3] Takšne drugotne epilepsije se pojavijo prek procesov tako imenovane epileptogeneze.[2][3] Vzročni mehanizem bi lahko bil tudi popustitev krvno-možganske pregrade, ob katerem bi snovi iz krvi prodrle v možgane.[101]
Napadi
[uredi | uredi kodo]Spoznava se, da epileptični napadi ponavadi niso naključni dogodki. Pogosto jih izzovejo dejavniki (»sprožilci«), kot so stres, čezmerno uživanje alkohola, utripajoča svetloba ali pomanjkanje spanca. Izraz »prag napada« označuje količino dražljaja, ki je potrebna, da izzove napad; ta prag je pri epilepsiji nižji kot običajno.[97]
Pri epileptičnih napadih se skupina nevronov začne prožiti na nenormalen, pretiran[28] in usklajen način.[2] To ustvari val depolarizacije, znan kot paroksizmalni depolarizacijski premik.[102] Žariščni napadi se začnejo v enem predelu možganov, generalizirani pa v obeh možganskih poloblah.[32] Nekatere vrste napadov lahko spremenijo strukturo, medtem ko imajo drugi le majhen učinek.[103] Gliozo, zmanjšanje števila nevronov in atrofijo določenih predelov možganov povezujejo z epilepsijo, vendar pa ni jasno, ali je epilepsija vzrok teh sprememb ali njihova posledica.[103]
Diagnoza
[uredi | uredi kodo]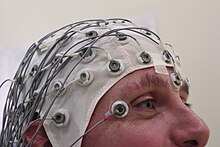
Diagnoza epilepsije se običajno postavi na podlagi opaženega poteka napada in njegovega temeljnega vzroka.[28] Del diagnostičnega postopka so običajno tudi elektroencefalografija (EEG), s katero se odkriva abnormalne vzorce v možganskih valovih, in nevroslikanje (računalniška tomografija ali MRI) za pregled strukture možganov.[28] Pogosto se poskuša prepoznati določen epileptični sindrom, vendar to ni vselej mogoče.[28] Pri zahtevnih primerih je lahko v pomoč video- in EEG-monitoring.[104]
Definicija
[uredi | uredi kodo]Epilepsija je možganska motnja, ki jo definira katerikoli izmed naslednjih pogojev:[12]
- Vsaj dva neizzvana (ali refleksna) napada, ki se zgodita v razmiku več kot 24 ur.
- En neizzvan (ali refleksni) napad in verjetnost novih napadov, podobna splošnemu tveganju ponovitve (vsaj 60 %), po dveh neizzvanih napadih v naslednjih 10 letih.
- Diagnoza epileptičnega sindroma.
Epilepsija velja za ozdravljeno pri posameznikih, ki so imeli starostno pogojen epileptični sindrom in so prerasli to starost, in pri tistih, ki niso imeli napada v zadnjih 10 letih, v zadnjih 5 letih pa niso jemali protiepileptičnih zdravil.[12]
Ta definicija Mednarodne lige proti epilepsiji[12] (ILAE) iz leta 2014 je prečiščena različica konceptualne definicije iste organizacije iz leta 2005, po kateri je epilepsija »motnja možganov, za katero je značilna trajna dovzetnost za tvorbo epileptičnih napadov ter nevrobiološke, kognitivne, psihološke in socialne posledice tega stanja. Za diagnozo epilepsije je potreben vsaj en epileptični napad.«[105][106]
Epilepsijo je potemtakem možno prerasti ali jo s terapijo ozdraviti, vendar brez zagotovila, da se ne bo znova pojavila. V definiciji se epilepsija zdaj imenuje bolezen in ne motnja; to je bila odločitev izvršnega odbora ILAE, ker naj bi beseda motnja, čeprav morda manj obremenjena s stigmo kot bolezen, ne izražala resnosti, ki si jo epilepsija zasluži.[12]
Definicija je po naravi praktična in zasnovana za klinično uporabo. Posebej je bil njen namen razjasniti, kdaj je prisotna »trajna dovzetnost«, ki jo navaja konceptualna definicija 2005. Raziskovalci, statistično naravnani epidemiologi in druge specializirane skupine se lahko odločijo uporabljati starejšo ali lastno definicijo. Za ILAE je to popolnoma dopustno, vse dokler je jasno razvidno, katera definicija je uporabljena.[12]
Definicija ILAE za en napad zahteva razumevanje projiciranja trajne dovzetnosti za tvorbo epileptičnih napadov.[12] Svetovna zdravstvena organizacija na primer uporablja le tradicionalno definicijo dveh neizzvanih napadov.[13]
Razvrstitev
[uredi | uredi kodo]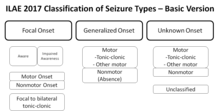
Za razliko od klasifikacije napadov, ki se osredotoča na dogajanje med napadom, se klasifikacija epilepsij osredotoča na njihove vzroke. Ko se oseba sprejme v bolnišnico po epileptičnem napadu, se, če je to mogoče, diagnosticira vrsta samega napada (npr. tonično-klonični) in njegov temeljni vzrok (npr. hipokampalna skleroza).[104] Ime naposled postavljene diagnoze je odvisno od razpoložljivih diagnostičnih rezultatov ter uporabljenih definicij in klasifikacij (napadov in epilepsij) ter odgovarjajoče terminologije.
Mednarodna liga proti epilepsiji (ILAE) je leta 2017 predlagala tristopenjsko klasifikacijo epilepsij in epileptičnih sindromov:[107] najprej se določi vrsto napada (po novi klasifikaciji napadov, izdani skupaj z novo klasifikacijo epilepsij[108]), nato se določi tip epilepsije in nazadnje se postavi diagnoza epileptičnega sindroma.[107] Novo uveden tip je kombinirana žariščna in generalizirana epilepsija, ki se določi pacientom z obema vrstama napadov.[107]
- stopnja: oblike napadov
- žariščni
- generalizirani
- neznano
- stopnja: tipi epilepsij
- žariščna epilepsija
- generalizirana epilepsija
- kombinirana žariščna in generalizirana epilepsija
- neznano
- stopnja: epileptični sindromi
- stopnja: oblike napadov
Ta klasifikacija je nadomestila predhodno klasifikacijo iz leta 1989,[109] ki dosegla splošno sprejetost po vsem svetu, bila pa je deležna tudi kritik, večinoma zato, ker ni podrobno obdelala temeljnih vzrokov epilepsije (ki so pomembna determinanta kliničnega postopka in prognoze).[110] To težavo je komisija ILAE prvič načela leta 2010 z razvrstitvijo epilepsij v tri kategorije (genetska, strukturalna/metabolna, neznan vzrok),[111] kar so v priporočilu leta 2011 prečistili v štiri kategorije in različne podkategorije.[112]
Klasifikacija iz leta 2017 je etiologijo vpela v vse korake klasifikacije, prepoznava pa šest etioloških skupin: strukturno, genetsko, infekcijsko, metabolno, imunsko in neznano. Posamezen primer epilepsije se lahko uvrsti v več kot eno skupino. Poleg tega se poudarja potreba po prepoznavi morebitnih pridruženih motenj, kot so učne, psihološke in vedenjske težave, ki se povezujejo z nekaterimi epilepsijami in lahko vplivajo na bolnika.[107]
Sindromi
[uredi | uredi kodo]Primeri epilepsije se po svojih značilnostih razvrščajo v epileptične sindrome. Te značilnosti so med drugim starost, pri kateri se začnejo napadi, vrsto napadov in izsledke EEG. Prepoznava epileptičnega sindroma je koristna za določitev temeljnih vzrokov in zdravil, s katerimi začeti zdravljenje.[32][113]
Možnost kategorizacije epilepsije v določen sindrom je večja pri otrocih.[69] Primeri manj resnih sindromov so benigna rolandična epilepsija (2,8 na 100 000), otroška epilepsija z absencami (0,8 na 100 000) in juvenilna mioklonična epilepsija (0,7 na 100 000).[69] Hude sindrome z razpršeno možgansko disfunkcijo, ki jih vsaj delno povzroča nek vidik epilepsije, imenujejo tudi razvojne in epileptične encefalopatije. Te se povezujejo s pogostimi napadi, ki se ne odzivajo na zdravljenje, in kognitivnimi motnjami, na primer Lennox-Gastautov sindrom (1–2 % vseh oseb z epilepsijo),[114] Dravetov sindrom (1 na 15 000–40 000 po svetu[115]) in Westov sindrom (1–9 na 100 000[116]).[117] Genetika pri epilepsiji verjetno igra pomembno vlogo prek več mehanizmov. Pri nekaterih so bili prepoznani preprosti in kompleksni modeli dedovanja. Po drugi strani obsežne presejalne raziskave niso odkrile veliko različic posameznih genov z velikim vplivom.[118] Novejše raziskave, v okviru katerih so sekvencirali eksome in genome, so pričele razkrivati številne de novo genske mutacije, odgovorne za nekatere epileptične encefalopatije, med njimi CHD2 in SYNGAP1[119][120][121] ter DNM1, GABBR2, FASN in RYR3.[122]
Sindrome, katerih vzroki niso jasno prepoznani, je težko uvrstiti v trenutno klasifikacijo epilepsije. Kategorizacija takšnih primerov je do neke mere arbitrarna.[112] Kategorija idiopatičnih (neznan vzrok) v klasifikaciji iz leta 2011 zajema sindrome, pri katerih splošne klinične značilnosti in/ali starostna specifičnost močno nakazujeta na domneven genetski vzrok.[112] V kategorijo neznanega vzroka so uvrščeni nekateri otroški epileptični sindromi, katerih vzrok naj bi bil genetski, na primer benigna rolandična epilepsija.[112] Klinične sindrome, katerih glavna značilnost ni epilepsija (npr. Angelmanov sindrom), so uvrstili med simptomatske, nekateri pa so zagovarjali njihovo vključitev v kategorijo idiopatskih.[112] Klasifikacija epilepsij in zlasti epileptičnih sindromov se bo z napredki raziskav spremenila.[112]
Preiskave
[uredi | uredi kodo]Elektroencefalogram (EEG) prikazuje aktivnost možganov, ki nakazuje povečano tveganje za napade. preiskava je priporočljiva le pri osebah, pri katerih na podlagi simptomov obstaja verjetnost za pojav epileptičnega napada. Pri diagnosticiranju epilepsije lahko elektroencefalografija pomaga določiti vrsto napada ali prisoten sindrom.[123] Pri otrocih je običajno potrebna le po drugem napadu, razen če drugače odloči specialist. Ne more služiti za izključitev diagnoze in lahko da lažen pozitiven rezultat pri osebah, ki nimajo epilepsije.[123] V določenih primerih je morda koristno opraviti EEG na posameznikih, ki spijo ali ki jim manjka spanca.[104]
Diagnostično slikanje s CT-jem in MRI je priporočljivo po prvem nevročinskem napadu za odkrivanje strukturnih težav v možganih in okoli njih.[104] Boljši način pregleda je na splošno MRI, razen kadar obstaja sum na krvavitev, ki jo CT zazna bolje in je lažje dostopen.[23] Če oseba pride na urgenco z napadom, a se hitro povrne v normalno stanje, se lahko slikanje opravi kasneje.[23] Če pa ima oseba anamnezo epilepsije in je slikanje že bilo opravljeno, ponovno slikanje običajno ni potrebno, tudi če se napadi ponavljajo.[104][124]
Pri odraslih je pomembno preverjanje ravni elektrolitov, glukoze v krvi in kalcija, da se ti izključijo kot vzrok napadov.[104] Z elektrokardiogramom je mogoče izključiti težave z motnjami srčnega ritma.[104] Punkcija v ledvenem predelu pomaga pri diagnosticiranju okužbe osrednjega živčevja, ni pa del rutinskega postopka.[23] Pri otrocih so lahko potrebna dodatna testiranja, npr. biokemijska analiza urina in testiranje krvi za ugotavljanje presnovnih motenj.[104][125] Poleg EEG in nevroslikanja postaja eden najpomembnejših načinov diagnoze epilepsije genetsko testiranje, s katerim se lahko doseže diagnoza pri ustreznem deležu posameznikov s hudo epilepsijo, tako pri otrocih kot pri odraslih.[126] Od oseb z negativnim genetskim testom je pri nekaterih genetske preiskave pomembno ponoviti ali znova analizirati po 2–3 letih.[127]
Visoka raven prolaktina v krvi prvih 20 minut po napadu pomaga potrditi epileptični napad za razliko od psihogenih neepileptičnih napadov.[128][129] Raven prolaktina v serumu je manj uporabna za ugotavljanje žariščnih napadov.[130] Če je raven v mejah normale, to ne izključuje možnosti epileptičnega napada,[129] prav tako pa prolaktin v serumu ne loči epileptičnih napadov od omedlevice.[131] Zato se tega pregleda ne priporoča uvrstiti med rutinske postopke pri diagnosticiranju epilepsije.[104]
Diferencialna diagnoza
[uredi | uredi kodo]Epilepsijo je pogosto težko diagnosticirati. Z znaki in simptomi, ki so zelo podobni epilepsiji, se lahko izrazijo številna druga stanja, med drugim omedlevica, hiperventilacija, migrene, narkolepsija, napadi panike in psihogeni neepileptični napadi (PNeN).[132][133] Zlasti omedlevico lahko spremlja kratkotrajen pojav konvulzij.[134] Nočna epilepsija frontalnega režnja, pogosto napačno razumljena kot nočne more, je nekoč veljala za motnjo spanja, pozneje pa so jo prepoznali za epileptičen sindrom.[135] Za epilepsijo je moč zamenjati napade paroksizmalne diskinezije, motnje gibanja.[136] Nenadne padce lahko med drugim povzroči tudi atonični napad.[133]
Nekatera vedenja otrok je mogoče zlahka zamenjati za epileptične napade. Primeri takega zavajajočega vedenja so med drugim afektivni krč, močenje postelje, nočni strahovi, tiki in napadi drgetanja.[133] Pri dojenčkih lahko gastroezofagealni refluks povzroči usločenje hrbta in zasuk glave vstran, kar je mogoče napačno razumeti kot tonično-klonični napad.[133]
Napačne diagnoze so pogoste (v okoli 5–30 % primerov).[28] Različne raziskave so pokazale, da imajo številni epileptičnim podobni napadi, ki se ne odzivajo na antiepileptike, kardiovaskularen vzrok.[134][137] Približno 20 % ljudi na epilepsijskih klinikah ima PNeN,[23] od teh pa jih ima okoli 10 % tudi epilepsijo.[138] Razlikovanje zgolj na podlagi napada brez nadaljnjih preiskav je pogosto zahtevno.[138]
Preventiva
[uredi | uredi kodo]Pri večini primerov preventiva ni možna, pomagajo pa zmanjševanje pogostosti poškodb glave,[7] dobra oskrba v času poroda in varovanje pred okoljskimi zajedavci, kot je svinjska trakulja.[18] V predelu Srednje Amerike so s prizadevanji za zmanjšanje stopnje pojavnosti svinjske trakulje zmanjšali število novih primerov epilepsije za 50 %.[22]
Zdravljenje
[uredi | uredi kodo]
Epilepsija se običajno zdravi z dnevnim jemanjem zdravil, potem ko se pojavi drugi napad,[28][104] osebe z visokim tveganjem pa zdravila lahko začnejo jemati že po prvem napadu.[104] Koristno je epileptikom nuditi podporo pri skrbi zase.[139] Pri bolnikih, pri katerih je bolezen odporna proti zdravljenju z zdravili, pridejo v poštev različne možnosti, na primer posebna dieta, vsaditev nevrostimulatorja ali nevrokirurški poseg.
Prva pomoč
[uredi | uredi kodo]Osebo, ki ima tonično-klonični napad, je treba obrniti na bok v položaj za nezavestnega, kar prepreči, da bi tekočina stekla v pljuča.[140] Osebi, ki ima napad, ni priporočljivo v usta dajati prstov, grizala ali jezičnega loparčka, da ne bi sprožili bruhanja oziroma da vas prizadeta oseba ne ugrizne.[30][140] Čim bolj je treba preprečiti samopoškodbe.[30] Imobilizacija hrbtenice običajno ni potrebna.[140]
Če napad traja dlje kot 5 minut ali če sta v eni uri več kot dva napada, ne da bi se med napadoma stanje povrnilo v normalno, se tak primer obravnava kot nujen primer, poimenovan epileptični status.[104][141] V tem primeru je lahko potrebna medicinska pomoč za ohranjanje prostih in zaščitenih dihalnih poti;[104] pri tem lahko pomaga nosno-žrelni tubus.[140] Doma je v primeru dolgotrajnega napada priporočljivo začetno zdravilo midazolam, ki se daje v nos ali usta.[142] Diazepam se lahko uporablja tudi rektalno.[142] V bolnišnicah se uporablja intravenski lorazepam.[104] Če dva odmerka benzodiazepina ne učinkujeta, je priporočljiva uporaba drugih zdravil, kot je fenitoin.[104] V primeru konvulzivnega epileptičnega statusa, ki se ne odziva na začetno zdravljenje, je potreben sprejem na intenzivno nego in zdravljenje z močnejšimi učinkovinami, kot so infuzija midazolama, ketamin, tiopenton ali propofol.[104]
Zdravila
[uredi | uredi kodo]
Kot glavno zdravljenje epilepsije se uporabljajo antiepileptiki, ki jih mora oseba morda jemati vse življenje.[28] Izbira antiepileptikov je odvisna od vrste napadov, sindroma epilepsije, drugih zdravil, ki jih oseba jemlje, njenih ostalih zdravstvenih težav, starosti in življenjskega sloga.[142] Na začetku se priporoča uporaba enega zdravila.[143] Če to ni učinkovito, ga je treba zamenjati z drugim zdravilom.[104] Jemanje dveh zdravil hkrati je priporočljivo le, če eno samo zdravilo ne učinkuje.[104] Pri približno polovici ljudi je učinkovita prva učinkovina, druga posamezna učinkovina pomaga pri približno 13 %, tretja oziroma dve učinkovini hkrati lahko pomagata pri dodatnih 4 %.[144] Pri okoli 30 % ljudi se kljub zdravljenju z antiepileptiki napadi še naprej pojavljajo.[7]
Na voljo so številna zdravila, med njimi fenitoin, karbamazepin in valproat. Obstajajo dokazi, da so omenjena zdravila lahko enako učinkovita tako pri žariščnih kot pri generaliziranih napadih.[145][146] Izkazalo se je, da karbamazepin z nadzorovanim sproščanjem deluje prav tako dobro kot karbamazepin s takojšnjim sproščanjem in ima lahko manj neželenih učinkov.[147] V Združenem kraljestvu se za primarno zdravljenje žariščnih napadov priporočata karbamazepin ali lamotrigin, levetiracetam in valproat pa zaradi stroškov in stranskih učinkov za drugotno zdravljenje.[104][148] Za generalizirane napade se kot primarno zdravilo priporoča valproat, lamotrigin pa kot drugotno zdravilo.[104] Pri ljudeh z odsotnostnimi napadi se priporoča uporaba etosuksimida ali valproata. Valproat je posebej učinkovit pri miokloničnih napadih in toničnih ter atoničnih napadih.[104] Če so napadi z določenim zdravljenjem dobro nadzorovani, običajno ni potrebe po rutinskem preverjanju ravni zdravil v krvi.[104]
Najcenejši antiepileptik je fenobarbital.[22] Svetovna zdravstvena organizacija ga priporoča kot zdravilo prvega izbora za države v razvoju in se tam redno uporablja.[149][150] Dostop do tega zdravila pa je lahko otežen, ker ga nekatere države označujejo kot nadzorovano zdravilo.[22]
O neželenih učinkih zdravil poroča 10 do 90 % ljudi, odvisno od tega, kdo je zbiral podatke in kako.[151] Večina neželenih učinkov je odvisnih od odmerka in so blagi.[151] Nekateri takšni neželeni učinki so nihanje razpoloženja, zaspanost in nestabilnost pri hoji.[151] Nekatera zdravila imajo neželene učinke, ki niso povezani z odmerjanjem, kot so na primer izpuščaji, strupenost za jetra ali supresija kostnega mozga.[151] Do ena četrtina oseb se zaradi neželenih učinkov odloči prekiniti zdravljenje.[151] Nekatera zdravila so povezana s prirojenimi napakami, če se jemljejo med nosečnostjo.[104] Za številna pogosto uporabljena zdravila, kot so valproat, fenitoin, karbamazepin, fenobarbital in gabapentin, obstajajo poročila o povečanem tveganju za prirojene napake,[152] posebno ob jemanju v prvih treh mesecih.[153] Kljub temu se zdravljenje, če je učinkovito, pogosto nadaljuje, saj je tveganje pri nezdravljenju epilepsije večje kot pa tveganje, če se zdravil ne jemlje.[153] Od protiepileptičnih zdravil naj bi levetiracetam in lamotrigin predstavljala najmanjše tveganje za prirojene napake.[152]
Postopno prenehanje jemanja zdravil je smiselno pri osebah, ki napadov nimajo že dve do štiri leta; vendar pa se napadi pri tretjini ljudi znova pojavijo, najpogosteje v prvih šestih mesecih.[104][154] Prenehanje jemanja zdravil je možno pri približno 70 % otrok in pri približno 60 % odraslih oseb.[18]
Operacija
[uredi | uredi kodo]Kirurško zdravljenje epilepsije je lahko možnost zdravljenja za vse osebe z epilepsijo, ki se ne odziva na zdravila.[155] Obravnava se vsak primer posebej v centrih, ki imajo izkušnje s kirurškim zdravljenjem epilepsije.[155] Izsledki pregleda iz leta 2023 so, da kirurški posegi pri 1 do 36 mesecev starih otrocih z na zdravila odporno epilepsijo lahko znatno zmanjšajo pogostost napadov ali jih odpravijo, posebej kjer so ostali načini zdravljenja odpovedali.[156] Kirurško zdravljenje epilepsije je lahko možnost za ljudi z žariščnimi napadi, ki ostajajo težava kljub drugim načinom zdravljenja,[157][158] od tega preizkušenima vsaj dvema ali tremi zdravili.[159] Cilj kirurškega posega je popoln nadzor nad napadi,[160] večina zdravnikov pa meni, da lahko tudi paliativna operacija, s katero se breme napadov znatno zmanjša, pomaga pri spodbujanju razvoja otrok z na zdravila odporno epilepsijo; to se doseže v 60–70 % primerov.[159] Običajni posegi so med drugim izrez hipokampusa z resekcijo sprednjega senčnega režnja, odstranitev tumorjev in odstranitev delov neokorteksa.[159] Nekateri posegi, kot je kalozotomija korpusa, se izvedejo kot poskus zmanjšanja števila napadov in ne kot poskus ozdravljenja stanja.[159] Po operaciji je pogosto možna postopna ukinitev zdravil.[157][159]
Nevrostimulacija
[uredi | uredi kodo]Za epileptike, pri katerih operacija ne pride v poštev, bi lahko bila možnost nevrostimulacija z implantacijo nevrokibernetske proteze, ki poleg običajne nege ustvarja stalno pulzirajočo električno stimulacijo določenega živca ali možganske regije.[104] Pri osebah, ki se ne odzivajo na zdravila, so se doslej izvajale tri vrste nevroterapije: spodbujanje vagusnega živca (VNS), anteriorna talamična stimulacija in odzivna stimulacija v zaprti zanki (RNS).[5][161][162]
Prehrana
[uredi | uredi kodo]Nekatere raziskave nakazujejo, da ketogena dieta (veliko maščob, malo ogljikovih hidratov in dovolj beljakovin) zmanjša pogostost napadov in jih pri nekaterih ljudeh odpravi, vendar pa so potrebne nadaljnje raziskave.[6] Pregledni članek iz leta 2022 navaja nekaj dokazov, da ketogena dieta ali prilagojena Atkinsova dieta lahko pomaga pri epilepsiji pri nekaterih dojenčkih.[163] Tovrstne diete so lahko koristne pri otrocih z epilepsijo, odporno na zdravila, njihovo delovanje pri odraslih pa ostaja negotovo.[6] Najpogostejši sporočeni stranski učinki so bili bruhanje, zaprtje in driska.[6] Zakaj dieta deluje, ni jasno.[164] Pri ljudeh s celiakijo ali neceliakalno preobčutljivostjo na gluten ter okcipitalno kalcifikacijo lahko pogostost napadov zmanjša brezglutenska dieta.[90]
Drugo
[uredi | uredi kodo]Terapija z izogibanjem pomeni, da se čim bolj zmanjšajo ali odstranijo sprožilci napadov. Pri osebah, ki so na primer občutljive na svetlobo, je lahko koristno, da imajo manjši televizor, se izogibajo videoigricam ali nosijo zatemnjena očala.[165] Zdravljenje s tehniko biološko-inštrumentalne povratne zveze na podlagi valov EEG je lahko koristen pri osebah, ki se ne odzivajo na zdravila.[166] Kljub temu psiholoških metod ni primerno uporabljati kot nadomestilo za zdravila.[104]
Za preprečevanje napadov nekateri predlagajo telesno vadbo,[167] kar podpirajo tudi nekatere raziskave.[168] Med ali po napadu lahko pomagajo psi, šolani za pomoč epileptikom.[169][170] Nejasno je, ali imajo psi zmožnost predvideti napade, preden se zgodijo.[171]
Srednje močni dokazi podpirajo uporabo psiholoških intervencij poleg drugih načinov zdravljenja.[172] Pri odraslih in mladostnikih lahko izboljšajo kakovost življenja, izboljšajo čustveno dobro počutje in zmanjšajo utrujenost.[172] Pri nekaterih posameznikih lahko izboljšajo nadzor nad napadi, saj spodbujajo skrb zase in upoštevanje podanih priporočil.[172]
Kot koristna dopolnilna terapija v primeru, da ostala zdravila ne obvladujejo napadov, se je pri nekaterih otrocih izkazal kanabidiol.[173][174] Leta 2018 je ameriška FDA odobrila njegovo uporabo pri Lennox-Gastautovem sindromu in Dravetovem sindromu.[175]
Obstaja nekaj raziskav o obvladovanju na zdravila odpornih napadov pri odraslih in pri otrocih z deksametazonom.[176]
Alternativna medicina
[uredi | uredi kodo]Za alternativno medicino, vključno z akupunkturo,[177] vitamini[178] in jogo,[179] ni zanesljivih dokazov, ki bi podprli njihovo uporabo pri epilepsiji. Melatonin (stanje 2016) ni zadostno podprt z dokazi;[180] dosedanji poskusi so bili metodološko šibki in iz njih ni bilo možno izpeljati zanesljivih zaključkov.[180]
Po nekaterih podatkih in različno podprta z dokazi naj bi bila pri epilepsiji, odporni na zdravila, koristna nekatera prehranska dopolnila. Med njimi so maščobne kisline omega-3, berberin, med manuka, gobe reiši in resasti bradovec, kurkumin,[181] vitamin E, koencim Q-10 in resveratrol. Teoretični razlog, zakaj delujejo, je zmanjševanje vnetij ali oksidativnega stresa, dveh velikih dejavnikov, ki pripomoreta k epilepsiji.[182]
Kontracepcija in nosečnost
[uredi | uredi kodo]Ženskam z epilepsijo se lahko začasno poveča pogostost napadov ob začetku hormonske kontracepcije.[183]
Nekateri antiepileptiki interagirajo z encimi v jetrih, zaradi česar se učinkovine hormonske kontracepcije hitreje razgradijo. Ta encime inducirajoča zdravila zmanjšujejo učinkovitost hormonske kontracepcije, kar je zlasti nevarno, če se zdravilo povezuje s prirojenimi okvarami.[184] Močna encime inducirajoča protiepileptična zdravila so med drugim karbamazepin, eslikarbazepin acetat, okskarbazepin, fenobarbital, fenitoin, primidon in rufinamid. Perampanel in topiramat lahko delujeta kot induktorja encimov pri višjih odmerkih.[185] Po drugi strani lahko hormonska kontracepcija zmanjša količino antiepileptika lamotrigina, ki kroži po telesu, in ga naredi manj učinkovitega.[183] Stopnja neučinkovitosti oralnih kontracepcijskih sredstev je ob pravilni uporabi 1 %, pri ženskah z epilepsijo pa znaša 3–6 %.[184] V splošnem se ženskam z epilepsijo, ki ne želijo zanositi, priporočajo intrauterini pripomočki.[183]
Ženske z epilepsijo imajo lahko, posebej v primeru drugih zdravstvenih posebnosti, rahlo nižjo, a še vedno visoko možnost zanositve.[183] Neplodne ženske imajo približno enako možnost uspeha oploditve z biomedicinsko pomočjo oziroma drugih tehnik asistirane reprodukcije kot ženske brez epilepsije.[183] Pojavi se lahko povečano tveganje izgube nosečnosti.[183]
Po začetku nosečnosti sta z njo povezani dve nevarnosti. Prva je tveganje napadov med nosečnostjo, druga pa prirojene napake, ki bi jih lahko povzročila protiepileptična zdravila.[152] Večina žensk z epilepsijo mora jemanje zdravil nadaljevati, cilj pa je uravnotežiti potrebo po preprečevanju napadov s potrebo po preprečevanju prirojenih okvar zaradi zdravil.[183][186]
Ni videti, da bi nosečnost resno vplivala na pogostost napadov.[183] Ko se napadi zgodijo, pa lahko povzročijo nekatere zaplete pri nosečnosti, kot sta predčasen porod ali neobičajno majhna velikost novorojenčkov.[183]
Tveganje za prirojene okvare obstaja pri vsaki nosečnosti, na primer zaradi kajenja,[183] poleg tega pa lahko nekatera protiepileptična zdravila znatno povečajo tveganje za okvare in za intrauterini zastoj rasti, kot tudi za razvojne, nevrokognitivne in vedenjske motnje.[186] Večina žensk z epilepsijo prejema varno in učinkovito zdravljenje ter ima zdrave otroke.[186] Največja tveganja so povezana z določenimi zdravili, kot sta valproična kislina in karbamazepin, in z višjimi odmerki.[152][183] Dodaten vnos folne kisline, na primer s predporodnimi vitaminskimi dopolnili, so tveganje zmanjšala.[183] Vnaprejšnje načrtovanje nosečnosti ženskam z epilepsijo omogoča, da preidejo na tretma manjšega tveganja in na manjše odmerke zdravil.[183]
Čeprav je protiepileptična zdravila mogoče zaznati v materinem mleku, ženske z epilepsijo lahko dojijo, koristi pa običajno prevladajo nad tveganji.[183]
Prognoza
[uredi | uredi kodo]
Epilepsije običajno ni mogoče pozdraviti, vendar lahko zdravila učinkovito nadzorujejo napade pri približno 70 odstotkih primerov.[7] Pri osebah z generaliziranimi napadi je nadzorovanje z zdravili uspešno pri 80 odstotkih, pri osebah z žariščnimi napadi pa je uspešnost 50-odstotna.[5] Eden od napovednikov dolgoročnega izida je število napadov, ki se pojavijo v prvih šestih mesecih.[28] Drugi dejavniki, ki povečujejo tveganje slabših rezultatov, vključujejo: majhen odziv na začetno zdravljenje, generalizirane napade, epilepsijo v družini, psihiatrične težave in valove na EEG, ki predstavljajo generalizirano epileptiformno dejavnost.[187] Po definiciji ILAE velja epilepsija za ozdravljeno, če oseba 10 let ni imela napada in 5 let ni jemala antiepileptikov.[188]
V državah v razvoju se 75 % ljudi ne zdravi oziroma se ne zdravi ustrezno.[18] V Afriki se ne zdravi 90 % prizadetih.[18] Razlog za to je med drugim, da ustrezna zdravila niso na voljo ali pa so predraga.[18]
Smrtnost
[uredi | uredi kodo]Ljudje z epilepsijo imajo povečano tveganje prezgodnje smrti,[189] ki naj bi bilo 1,6- do 4,1-krat večje kot pri splošni populaciji.[190] Največji porast smrtnosti zaradi epilepsije je pri starejših osebah.[190] Osebe, ki imajo epilepsijo z nepojasnjenim vzrokom, imajo le rahlo povečano tveganje.[190]
Smrtnost je pogosto povezana z osnovnim vzrokom napadov, statusom epilepticusom (SE), samomorom, travmami in nenadno nepričakovano smrtjo pri epilepsiji (angl. »sudden unexpected death in epilepsy« – SUDEP).[189] Smrtnost zaradi statusa epilepticusa je najvišja v skupini bolnikov, kjer je do SE privedlo predobstoječe bolezensko stanje (hipoksija centralnega živčevja po srčnem zastoju, okužba centralnega živčevja ali cerebrovaskularna bolezen, navadno možganska kap) tj. sekundarna epilepsija, v razvitem svetu smrt redkeje nastopi zaradi SE pri bolnikih s primarno (tj. nevzročno) epilepsijo.[189] Tveganje samomora je pri ljudeh z epilepsijo povečano za dva- do šestkrat;[191][192] razlog za to je nejasen.[191] Nenadna nepričakovana smrt pri epilepsiji je lahko delno povezana s pogostostjo generaliziranih tonično-kloničnih napadov[193] in je vzrok približno 15 % smrti, povezanih z epilepsijo;[187] kako zmanjšati tveganje zanjo, ni znano.[193] Med dejavniki tveganja za nenadno nepričakovano smrt so nočni generalizirani tonično-klonični napadi, samostojno spanje in na zdravila odporna epilepsija.[194]
V Združenem kraljestvu ocenjujejo, da bi bilo možno preprečiti 40–60 % smrti.[28] V državah v razvoju številnim smrtim botruje nezdravljena epilepsija, ki privede do padcev ali statusa epilepticusa.[22]
Epidemiologija
[uredi | uredi kodo]Epilepsija je ena najpogostejših resnih nevroloških motenj,[195] ki je leta 2021 prizadevala približno 50 milijonov ljudi.[8][196] Pojavi se pri 1 % prebivalstva do 20. leta starosti in pri 3 % prebivalstva do 75. leta starosti.[20] Pogostejša je pri moških kot pri ženskah, čeprav je skupna razlika majhna.[22][69] Večina obolelih (80 %) je v družbah z nizkimi prihodki[197] in v državah v razvoju.[18] V Sloveniji je bila prevalenca epilepsije leta 2010 ocenjena na 10 030 oseb.[16]
Ocenjeno je bilo (2012), da ima aktivno epilepsijo približno 3–10 na 1000 oseb, pri čemer je bila aktivna epilepsija opredeljena kot epilepsija, pri kateri se je v zadnjih petih letih pojavil vsaj en neizzvan napad.[69][198] Epilepsija se vsako leto začne pri 40–70 na 100 000 ljudi v razvitih državah in pri 80–140 na 100 000 ljudi v državah v razvoju.[18] Revščina je tveganje in vključuje tako dejstvo, da prizadeti prihaja iz revne države, kot tudi dejstvo, da je revnejši v primerjavi z drugimi v svoji državi.[22] V razvitem svetu se epilepsija najpogosteje začne pri mlajših ali pri starejših.[22] V državah v razvoju se bolezen pogosto začne pri starejših otrocih in mladih odraslih zaradi več primerov travm in infekcijskih bolezni.[22] V razvitih državah se je od 70. let dvajsetega stoletja do leta 2003 število primerov na leto pri otrocih zmanjšalo, povečalo pa se je število primerov pri starejši populaciji.[198] To gre deloma pripisati boljšemu preživetju po kapi pri odraslih.[69]
Zgodovina
[uredi | uredi kodo]Najstarejši medicinski zapisi kažejo, da se je epilepsija pri ljudeh pojavljala vsaj od začetka beleženja zgodovine.[199] V starem veku so motnji pripisovali duhoven vzrok.[199] Najstarejši opis epileptičnega napada na svetu je v akadščini (jeziku v stari Mezopotamiji), napisan pa je bil okrog 2000 pr. n. št.[10] Za osebo so zapisali, da je pod vplivom boga lune, in so jo zdravili z izganjanjem duhov.[10] Epileptične napade omenja tudi Hamurabijev zakonik (okrog 1790 pr. n. št.) kot upravičen razlog za vrnitev kupljenega sužnja,[10] in papirus Edwina Smitha (okrog 1700 pr. n. št.), ki opisuje primere posameznikov z epileptičnimi krči.[10]
Najstarejši znan podroben zapis o motnji sami je v Sakikkūju, babilonskem medicinskem besedilu v klinopisu iz 1067–1046 pr. n. št.[199] Besedilo opisuje znake in simptome, razlaga zdravljenje in možne izide[10] ter opisuje številne lastnosti različnih vrst napadov.[199] Ker Babilonci niso razumeli narave te bolezni, so napade pojasnjevali kot obsedenost z zlimi duhovi in epilepsijo zdravili na duhovne načine.[199] Okrog 900 pr. n. št. je vedež Punarvasu Ātreya epilepsijo opisal kot izgubo zavesti,[200] to definicijo pa vsebuje tudi ajurvedsko besedilo Čaraka samita (okrog 400 pr. n. št.).[201]

Grki so imeli o bolezni nasprotujoča mnenja. Po eni strani so menili, da je epilepsija neke vrste obsedenosti duha, po drugi strani pa da gre lahko za stanje, povezano z genialnostjo in božanskostjo. Eno od imen, pod katerimi so jo poznali, je »sveta bolezen«. Epilepsija nastopa v grški mitologiji: povezovali so jo z boginjama Lune Seleno in Artemido, ki sta z njo kaznovali vsakogar, ki si ju je upal vznemiriti. Grki so menili, da imajo tako bolezen pomembni ljudje, kot sta na primer bila Julij Cezar in Herkul.[10] Opazna izjema pri tem božanskem in duhovnem razlaganju je bila Hipokratova šola. V petem stoletju pred našim štetjem je Hipokrat zavrnil mnenje, da bolezen povzročajo duhovi. V svojem prelomnem delu »O sveti bolezni« je zapisal mnenje, da epilepsija ni božanskega izvora, temveč da gre za medicinsko ozdravljiv problem, ki izvira iz možganov.[10][199] Tiste, ki so bolezni pripisovali sveti vzrok, je obtožil širjenja nevednosti in vere v vraževerno magijo.[10] Hipokrat je menil, da je kot vzrok pomembna dednost, opisal je slabše napovedi, če se bolezen pojavi v zgodnjem otroštvu, in navedel njene telesne lastnosti, pa tudi družbeno sramoto, ki je z njo povezana.[10] Namesto »sveta bolezen« jo je imenoval »velika bolezen«, iz česar izhaja dandanašnje ime »grand mal«, ki se uporablja za tonično-klonične napade.[10] Kljub temu, da je podrobno opisal telesne izvore bolezni, njegovi sodobniki njegovega mnenja niso sprejeli.[199] Za bolezen so še v 17. stoletju krivili zle duhove.[199]
V antičnem Rimu ljudje niso jedli in pili iz iste posode kot prizadeti.[202] Tedanji ljudje so pljuvali pred epileptike in verjeli, da jih bolezen tako ne bo prizadela.[202] Po pričevanjih Apuleja in drugih antičnih zdravnikov so epilepsijo običajno odkrivali tako, da so prižgali kos gagata, katerega dim naj bi sprožil napad.[203] Občasno so za to uporabljali vrteče se lončarsko vreteno, ki je verjetno sprožilo napade pri ljudeh, občutljivih na svetlobo.[204]
Večina kultur je osebe z epilepsijo stigmatizirala, se jih izogibala ali pa celo zapirala. Celo v drugi polovici 20. stoletja so v Tanzaniji in drugih predelih Afrike epilepsijo povezovali z obsedenostjo z zlimi duhovi, s čarovništvom ali zastrupitvami ter verjeli, da je nalezljiva.[205] V Salpêtrièru, rojstnem kraju sodobne nevrologije, je Jean-Martin Charcot našel epileptike v istih prostorih z bolniki, ki so bili duševno prizadeti, ki so imeli kroničen sifilis in ki so bili kazensko nori.[206] V antičnem Rimu je bila epilepsija znana kot morbus comitialis ali »zbornična bolezen« in veljala za božje prekletstvo. V severni Italiji so epilepsijo poznali kot bolezen sv. Valentina.[207] Vsaj v 40. letih 19. stoletja so v Združenih državah Amerike epilepsijo poznali kot falling sickness ali the falling fits in jo imeli za obliko medicinske norosti.[208] V približno istem času so v Franciji epilepsijo imenovali haut-mal (»visoko zlo«), mal-de terre (»zemeljska bolezen«), mal de Saint Jean (»bolezen sv. Janeza«), mal des enfans (»otroška bolezen«) in mal-caduc (»bolezen padanja«).[208] Epileptiki v Franciji so bili znani kot tombeurs (»padajoči«) zaradi napadov in izgub zavesti.[208] Enako je nastalo slovensko poimenovanje padavica, iz prepričanja o nadnaravnih razlogih za napad pa božjast, ki v novejšem času izginjata iz rabe.[11]
Sredi 19. stoletja so odkrili in uvedli bromid, to je prvo zdravilo, ki je bilo uspešno proti napadom.[151] Prvo sodobno zdravilo, fenobarbital, so razvili leta 1912, fenitoin pa se je začel uporabljati leta 1938.[209]
Družba in kultura
[uredi | uredi kodo]Stigma
[uredi | uredi kodo]Ljudje z epilepsijo so po svetu pogosto stigmatizirani.[13][210] Epilepsija jih prizadene gospodarsko, socialno in kulturno.[210] V Indiji in na Kitajskem je epilepsija lahko utemeljitev za zavrnitev zakonske zveze.[18] Ponekod še vedno verjamejo, da so ljudje z epilepsijo zakleti.[22] V delih Afrike, kot sta Tanzanija in Uganda, epilepsijo razlagajo kot obsedenost s zlimi duhovi, čarovništvo, ali zastrupljenje; veliko ljudi tudi verjame, da je nalezljiva.[22][205] Do leta 1971 je bilo v Združenem kraljestvu s sklicevanjem na epilepsijo možno doseči razveljavitev zakonske zveze.[18] Zaradi stigme lahko nekateri ljudje z epilepsijo zanikajo, da bi kdajkoli imeli epileptične napade.[69] Presečna raziskava iz leta 2024 je odkrila, da je 64,8 % sorodnikov epileptikov že doživelo zmerno stigmo in imajo do epilepsije zmerno pozitiven odnos. Raziskava je pri sodelujočih ugotovila povezavo med višjo stopnjo stigmatiziranosti in negativnejšim pogledom na bolezen. Poleg tega so se sorodniki oseb, ki doživljajo pogoste napade (enega ali več na mesec), soočali z večjo stigmo, sorodniki oseb, ki predpisanih zdravil ne jemljejo dosledno, pa so do epilepsije izkazovali negativnejši odnos.[211]
Gospodarstvo
[uredi | uredi kodo]Epilepsija je v letu 2010 v Sloveniji povzročila stroške v skupni vrednosti okoli 35,8 milijonov evrov (prilagojenih na pariteto kupne moči), od tega so 19,1 milijona predstavljali neposredni zdravstveni stroški.[16] V EU so bili skupni stroški za leto 2010 ocenjeni na 14 milijard €, od tega je na neposredne zdravstvene stroške odpadla slaba polovica.[16] V ZDA se neposredni stroški ocenjujejo na približno eno milijardo dolarjev,[23] v Indiji pa na 1,7 milijarde USD ali 0,5 % BDP.[18] V Združenih državah Amerike predstavlja vzrok približno 1 odstotka obiskov na urgentnem oddelku (2 odstotka na pediatričnih urgencah).[212]
Vozila
[uredi | uredi kodo]Osebe z epilepsijo imajo približno dvakrat večje tveganje, da bodo vpletene v prometno nesrečo, zato v mnogih državah po svetu ne smejo voziti ali pa smejo voziti le pod določenimi pogoji.[26] Kot vzrok nekaterih prometnih nesreč, ki bi se jim bilo možno izogniti, se izpostavlja nepravočasna diagnoza, vsaj ena študija je namreč pokazala, da so v večino prometnih nesreč vpleteni udeleženci z nediagnosticiranimi nemotoričnimi napadi in ne udeleženci z motoričnimi napadi ob diagnosticirani epilepsiji.[213] Ponekod so po zakonu zdravniki dolžni osebe z napadi prijaviti uradu za izdajanje dovoljenj, drugod pa so dolžni prizadeti osebi le svetovati, naj to prijavi sama.[26] Države, kjer se od zdravnikov zahteva poročanje, so med drugim Avstrija, Danska, Švedska in Španija.[26] V Združenem kraljestvu, Novi Zelandiji in nekaterih drugih državah se je posameznik obvezan sam prijaviti in zdravnik sme sam poslati obvestilo, če meni, da prizadeti tega še ni storil.[26] V Kanadi, ZDA in Avstraliji so zahteve glede poročanja odvisne od province oziroma zvezne države.[26]
Če so napadi zanesljivo pod nadzorom, je večina mnenja, da je vožnjo smiselno dovoliti.[214] Koliko časa mora oseba biti brez epileptičnih napadov, preden lahko vozi, je od države do države različno;[214] večina držav zahteva obdobje od enega do treh let.[214] V Sloveniji se vozniku z epilepsijo lahko ob pozitivnem mnenju specialista izda zdravniško spričevalo, če je brez napada vsaj eno leto (nekdaj vsaj dve leti).[215][216]
Ljudje z epilepsijo ali napadi običajno ne morejo dobiti pilotske licence.[217] V Kanadi lahko oseba, ki je imela en sam napad, po petih letih zahteva, da se ji, če so vsi drugi testi normalni, izda dovoljenje z omejitvami.[218] To velja tudi za ljudi, ki imajo vročinske krče in z zdravili povezane napade.[218] Zvezna uprava za letalstvo ZDA ne dovoljuje, da bi osebe z epilepsijo dobile dovoljenje za poklicnega pilota.[219] Redko se lahko naredijo izjeme za osebe, ki so imele en sam napad ali vročinske krče in ki so ostali brez napadov in brez zdravil vse do odrasle dobe.[220] V Združenem kraljestvu za nacionalno licenco zasebnega pilota veljajo isti pogoji kot za poklicno vozniško dovoljenje.[221] Pogoj je desetletno obdobje brez napadov in brez zdravil.[222] Tisti, ki ne izpolnjujejo te zahteve, lahko dobijo, če so pet let brez epileptičnih napadov, dovoljenje z omejitvami.[221]
Podporne organizacije
[uredi | uredi kodo]Obstajajo številne organizacije, ki pomagajo ljudem in družinam, prizadetih zaradi epilepsije. Mednarodno prizadevanje za večje poznavanje bolezni je med drugim kampanja »Ven iz sence«, v kateri sodelujejo Svetovna zdravstvena organizacija, Mednarodna liga proti epilepsiji in Mednarodni urad za epilepsijo.[18] V Sloveniji deluje prostovoljno nepridobitno društvo Liga proti epilepsiji Slovenije.[223]
Svetovni dan epilepsije se od leta 2015 obeležuje na drugi ponedeljek v februarju.[224][225] Drugi dan, namenjen osveščanju o epilepsiji, je »vijoličasti dan«, katerega tradicijo je leta 2008 začela devetletna Kanadčanka Cassidy Megan in se obeležuje vsako leto 26. marca.[226]
Raziskave
[uredi | uredi kodo]Napovedovanje in modeliranje napadov
[uredi | uredi kodo]Napovedovanje
[uredi | uredi kodo]Raziskuje se, ali je epileptične napade mogoče napovedati, preden se zgodijo, na podlagi elektroencefalograma.[227] Leta 2011 učinkovit način napovedovanja napadov še ni bil znan.[227] Čeprav pripomoček, ki bi zmogel napovedovati napade, ne obstaja, znanost pri napovedovanju napadov in razvoju takšne naprave napreduje.
Modeliranje
[uredi | uredi kodo]S tehniko, znano kot »kindling« – ponavljajočimi se izpostavitvami možnim sprožilcem napadov, po katerih se poveča dovzetnost za napade – so razvili več živalskih modelov epilepsije.[228] Pri glodavcih je bilo opisanih več modelov, ki povzemajo EEG in spremljajoče vedenjske pojave pri različnih oblikah epilepsije, posebej obstoj ponavljajočih se spontanih napadov.[229] Ker se pri nekaterih izmed teh živali v naravi pojavljajo raznovrstni epileptični napadi, so kot genetske modele za epilepsijo določili linije miši in podgan. Pri nekaterih linijah miši in podgan so na posnetih elektroencefalogramih razbrali razelektritve trn-val ter na njih raziskali absenčno epilepsijo.[230] Z enim izmed živalskih modelov, GAERS (Genetic Absence Epilepsy Rats from Strasbourg), opisanim v 80. letih prejšnjega stoletja, so dognali mehanizme, na katerih temelji otroška absenčna epilepsija.[231]
Rezine podganjih možganov služijo kot dragocen model za ocenjevanje, ali različne spojine omogočajo zmanjšanje epileptiformne aktivnosti. Z ocenjevanjem pogostosti epileptiformnih izbruhov v področju hipokampusa raziskovalci prepoznavajo potencialne spojine, ki bi jih lahko uporabili kot nova protiepileptična zdravila.[232]
Redukcionistični pogledi na epileptiformne razelektritve se pogosto izražajo z matematičnimi modeli. Najpreprostejši med njimi temeljijo na nekaj običajnih diferencialnih enačbah, takšen je na primer model Epileptor.[233] Bolj fiziološko usmerjen model Epileptor-2[234] replicira kratkotrajne razelektritve med dvema epileptičnima napadoma (mediktične) – zaznane kot sklope akcijskih potencialov posameznih nevronov – in daljše razelektritve med samim napadom (iktične), ki jih predstavljajo sklopi posameznih krajših razelektritev. Po tem modelu so kratke mediktične razelektritve okarakterizirane kot stohastična nihanja membranskega potenciala in sinaptične aktivnosti, medtem ko iktične razelektritve nastanejo kot nihanja v zunajcelični koncentraciji kalijevih ionov in v znotrajcelični koncentraciji natrijevih ionov. Ti modeli izkazujejo,[235] da pretok ionov igra odločilno vlogo v generiranju patološke aktivnosti.
Ena izmed hipotez, zastopanih v literaturi, temelji na vnetnih poteh. Raziskave, ki ta mehanizem podpirajo, so ugotavljale, da obstaja statisčno značilna povezava med vnetjem, zastopanostjo glikolipidov in oksidativnih faktorjev ter epilepsijo, zlasti generalizirano.[236]
Možne prihodnje terapije
[uredi | uredi kodo]Za nekatere vrste epilepsije se preučuje možnost genskega zdravljenja.[237] Zdravila, ki spremenijo imunsko funkcijo, kot so intravenski imunoglobulini, bi (upoštevajoč vnetno teorijo nastanka epilepsije) kot dopolnilo običajnemu zdravljenju lahko zmanjšala pogostost napadov; potrebno pa je raziskati, ali ta zdravila otroci in odrasli z epilepsijo dobro prenašajo.[238] Neinvazivna stereotaktična radiokirurgija se (stanje za leto 2012) za nekatere vrste epilepsije proučuje kot alternativa standardnim kirurškim metodam.[239]
Druge živali
[uredi | uredi kodo]Epilepsija se pojavlja pri številnih drugih živalih, med drugim pri psih in mačkah, in je pri psih najpogostejša možganska bolezen.[240] Običajno se jo zdravi z antikonvulzivi, kot so levetiracetam, fenobarbital ali bromid pri psih in fenobarbital pri mačkah.[240] Pri psih se uporablja tudi imepitoin.[241] Pri konjih je generalizirane napade dokaj enostavno diagnosticirati, teže pa je pri negeneraliziranih napadih, pri katerih je lahko koristen EEG.[242] Juvenilna idiopatska epilepsija (JIE) pri žrebetih se lahko razvije različno, odvisno od resnosti in zdravljenja. Nekatere živali jo sčasoma prerastejo brez bistvenih dolgoročnih učinkov, druge pa imajo lahko v primeru nepravočasnega zdravljenja hude posledice, vključno s smrtjo ali trajnimi zapleti. Raziskave so nakazale, da ima pri razvoju JIE pomemben vpliv genetika in da se motnja deduje po zakonitostih monogenskega dedovanja. Te ugotovitve poudarjajo potrebo po nadaljnjih genetskih raziskavah, ki bi potrdile to hipotezo, in po iskanju možnih strategij parjenja, s katerimi bi zmanjšali prevalenco JIE.[243]
Sklici
[uredi | uredi kodo]- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 1,7 »Epilepsy Fact sheet«. Svetovna zdravstvena organizacija. Februar 2016. Arhivirano iz spletišča dne 11. marca 2016. Pridobljeno 4. marca 2016.
- ↑ 2,00 2,01 2,02 2,03 2,04 2,05 2,06 2,07 2,08 2,09 2,10 2,11 2,12 McPhee, Stephen J.; Hammer, Gary D., ur. (2010). »7«. Pathophysiology of disease: an introduction to clinical medicine (6. izd.). New York: McGraw-Hill Medical. ISBN 978-0-07-162167-0.
- ↑ 3,0 3,1 3,2 Goldberg EM, Coulter DA (Maj 2013). »Mechanisms of epileptogenesis: a convergence on neural circuit dysfunction«. Nature Reviews. Neuroscience. 14 (5): 337–349. doi:10.1038/nrn3482. PMC 3982383. PMID 23595016.
- ↑ 4,0 4,1 4,2 4,3 4,4 Longo DL (2012). »369 Seizures and Epilepsy«. Harrison's principles of internal medicine (18th izd.). McGraw-Hill. str. 3258. ISBN 978-0-07-174887-2.
- ↑ 5,0 5,1 5,2 5,3 Bergey, GK (Junij 2013). »Neurostimulation in the treatment of epilepsy«. Experimental neurology. 244: 87–95. doi:10.1016/j.expneurol.2013.04.004. PMID 23583414.
- ↑ 6,0 6,1 6,2 6,3 6,4 Martin-McGill KJ, Bresnahan R, Levy RG, Cooper PN (Junij 2020). »Ketogenic diets for drug-resistant epilepsy«. The Cochrane Database of Systematic Reviews. 2020 (6): CD001903. doi:10.1002/14651858.CD001903.pub5. PMC 7387249. PMID 32588435.
- ↑ 7,0 7,1 7,2 7,3 7,4 Eadie, MJ (december 2012). »Shortcomings in the current treatment of epilepsy«. Expert review of neurotherapeutics. 12 (12): 1419–27. doi:10.1586/ern.12.129. PMID 23237349.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 8,0 8,1 »GBD 2021 Cause and Risk Summary: EPILEPSY«. Institute for Health Metrics and Evaluation (IHME). Seattle, USA: University of Washington. 2021. Arhivirano (PDF) iz spletišča dne 19. julija 2024. Pridobljeno 19. julija 2024.
- ↑ Sinmetz JD, Seeher KM, Schiess N, Nichols E, Cao B, Servili C, in sod. (1. april 2024). »Global, regional, and national burden of disorders affecting the nervous system, 1990–2021: a systematic analysis for the Global Burden of Disease Study 2021«. The Lancet Neurology. Elsevier. 23 (4): 344–381. doi:10.1016/S1474-4422(24)00038-3. hdl:1959.4/102176. PMC 10949203. PMID 38493795.
{{navedi časopis}}: Check|pmid=value (pomoč); Preveri|pmc=vrednost (pomoč) - ↑ 10,00 10,01 10,02 10,03 10,04 10,05 10,06 10,07 10,08 10,09 10,10 Magiorkinis E; Kalliopi S; Diamantis A (Januar 2010). »Hallmarks in the history of epilepsy: epilepsy in antiquity«. Epilepsy & behavior : E&B. 17 (1): 103–108. doi:10.1016/j.yebeh.2009.10.023. PMID 19963440.
- ↑ 11,0 11,1 »Enakovredni ali neenakovredni sopomenki: »božjast« in »epilepsija««. Jezikovna svetovalnica. Januar 2020. Pridobljeno 29. januarja 2025.
- ↑ 12,0 12,1 12,2 12,3 12,4 12,5 12,6 Fisher RS, Acevedo C, Arzimanoglou A, Bogacz A, Cross JH, Elger CE, Engel J, Forsgren L, French JA, Glynn M, Hesdorffer DC, Lee BI, Mathern GW, Moshé SL, Perucca E, Scheffer IE, Tomson T, Watanabe M, Wiebe S (april 2014). »ILAE official report: a practical clinical definition of epilepsy«. Epilepsia. 55 (4): 475–482. doi:10.1111/epi.12550. PMID 24730690.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 13,0 13,1 13,2 »Epilepsy«. Svetovna zdravstvena organizacija (v angleščini). Pridobljeno 1. aprila 2023.
- ↑ 14,0 14,1 Fisher R; van Emde Boas W; Blume W; Elger C; Genton P; Lee P; Engel J (2005). »Epileptic seizures and epilepsy: definitions proposed by the International League Against Epilepsy (ILAE) and the International Bureau for Epilepsy (IBE)«. Epilepsia. 46 (4): 470–2. doi:10.1111/j.0013-9580.2005.66104.x. PMID 15816939. Arhivirano iz prvotnega spletišča dne 27. septembra 2019. Pridobljeno 4. septembra 2007.
- ↑ 15,0 15,1 15,2 15,3 15,4 15,5 15,6 Pandolfo M (november 2011). »Genetics of epilepsy«. Seminars in Neurology. 31 (5): 506–518. doi:10.1055/s-0031-1299789. PMID 22266888.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 16,0 16,1 16,2 16,3 Bon, Jurij; Koritnik, Blaž; Bresjanac, Mara; Repovš, Grega; Pregelj, Peter; Dobnik, Bogdan; Pirtošek, Zvezdan (2013). »Stroški možganskih bolezni v Sloveniji v letu 2010«. Zdravniški vestnik. 82: 171.
- ↑ 17,0 17,1 Thurman DJ, Beghi E, Begley CE, Berg AT, Buchhalter JR, Ding D, Hesdorffer DC, Hauser WA, Kazis L, Kobau R, Kroner B, Labiner D, Liow K, Logroscino G, Medina MT, Newton CR, Parko K, Paschal A, Preux PM, Sander JW, Selassie A, Theodore W, Tomson T, Wiebe S (september 2011). »Standards for epidemiologic studies and surveillance of epilepsy«. Epilepsia. 52 (Suppl 7): 2–26. doi:10.1111/j.1528-1167.2011.03121.x. PMID 21899536.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 18,00 18,01 18,02 18,03 18,04 18,05 18,06 18,07 18,08 18,09 18,10 18,11 18,12 18,13 18,14 18,15 »Epilepsy«. Fact Sheets. World Health Organization. Oktober 2012. Pridobljeno 24. januarja 2013.
- ↑ Brodie, MJ; Elder, AT; Kwan, P (november 2009). »Epilepsy in later life«. Lancet neurology. 8 (11): 1019–30. doi:10.1016/S1474-4422(09)70240-6. PMID 19800848.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 20,0 20,1 Holmes, Thomas R. Browne, Gregory L. (2008). Handbook of epilepsy (4. izd.). Philadelphia: Lippincott Williams & Wilkins. str. 7. ISBN 978-0-7817-7397-3.
- ↑ Wyllie's treatment of epilepsy : principles and practice (5. izd.). Philadelphia: Wolters Kluwer/Lippincott Williams & Wilkins. 2010. ISBN 978-1-58255-937-7.
- ↑ 22,00 22,01 22,02 22,03 22,04 22,05 22,06 22,07 22,08 22,09 22,10 22,11 Newton CR, Garcia HH (september 2012). »Epilepsy in poor regions of the world«. Lancet. 380 (9848): 1193–1201. doi:10.1016/S0140-6736(12)61381-6. PMID 23021288.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 23,0 23,1 23,2 23,3 23,4 23,5 Wilden JA, Cohen-Gadol AA (Avgust 2012). »Evaluation of first nonfebrile seizures«. American Family Physician. 86 (4): 334–340. PMID 22963022.
- ↑ Neligan A, Adan G, Nevitt SJ, Pullen A, Sander JW, Bonnett L, Marson AG, in sod. (Cochrane Epilepsy Group) (Januar 2023). »Prognosis of adults and children following a first unprovoked seizure«. The Cochrane Database of Systematic Reviews. 1 (1): CD013847. doi:10.1002/14651858.CD013847.pub2. PMC 9869434. PMID 36688481.
- ↑ Epilepsy: what are the chances of having a second seizure? (poročilo). 16. avgust 2023. doi:10.3310/nihrevidence_59456.
- ↑ 26,0 26,1 26,2 26,3 26,4 26,5 L Devlin A, Odell M, L Charlton J, Koppel S (december 2012). »Epilepsy and driving: current status of research«. Epilepsy Research. 102 (3): 135–152. doi:10.1016/j.eplepsyres.2012.08.003. PMID 22981339.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 27,0 27,1 Duncan, JS; Sander, JW; Sisodiya, SM; Walker, MC (1. april 2006). »Adult epilepsy« (PDF). Lancet. 367 (9516): 1087–100. doi:10.1016/S0140-6736(06)68477-8. PMID 16581409. Arhivirano iz prvotnega spletišča (PDF) dne 24. marca 2013. Pridobljeno 30. marca 2014.
- ↑ 28,00 28,01 28,02 28,03 28,04 28,05 28,06 28,07 28,08 28,09 28,10 28,11 28,12 28,13 28,14 28,15 28,16 28,17 National Clinical Guideline Centre (Januar 2012). The Epilepsies: The diagnosis and management of the epilepsies in adults and children in primary and secondary care (PDF). National Institute for Health and Clinical Excellence. str. 21–28. Arhivirano (PDF) iz spletišča dne 16. decembra 2013.
- ↑ Hughes, JR (Avgust 2009). »Absence seizures: a review of recent reports with new concepts«. Epilepsy & behavior : E&B. 15 (4): 404–12. doi:10.1016/j.yebeh.2009.06.007. PMID 19632158.
- ↑ 30,0 30,1 30,2 30,3 Shearer, Peter. »Seizures and Status Epilepticus: Diagnosis and Management in the Emergency Department«. Emergency Medicine Practice.
- ↑ 31,0 31,1 31,2 31,3 Bradley, Walter G. (2012). »67«. Bradley's neurology in clinical practice (6. izd.). Philadelphia, PA: Elsevier/Saunders. ISBN 978-1-4377-0434-1.
- ↑ 32,0 32,1 32,2 32,3 32,4 National Clinical Guideline Centre (Januar 2012). The Epilepsies: The diagnosis and management of the epilepsies in adults and children in primary and secondary care (PDF). National Institute for Health and Clinical Excellence. str. 119–129.
- ↑ 33,0 33,1 33,2 Engel, Jerome (2008). Epilepsy : a comprehensive textbook (2. izd.). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. str. 2797. ISBN 978-0-7817-5777-5.
- ↑ 34,0 34,1 34,2 Simon DA, Greenberg MJ, Aminoff RP (2012). »12«. Clinical neurology (8th izd.). New York: McGraw-Hill Medical. ISBN 978-0-07-175905-2.
- ↑ 35,0 35,1 Stephenson JB (1990). Fits and faints. London: Mac Keith Press. ISBN 0-632-02811-4. OCLC 25711319.
- ↑ 36,0 36,1 Steven C. Schachter, ur. (2008). Behavioral aspects of epilepsy: principles and practice ([Online-Ausg.]. izd.). New York: Demos. str. 125. ISBN 978-1-933864-04-4.
- ↑ Xue LY, Ritaccio AL (Marec 2006). »Reflex seizures and reflex epilepsy«. American Journal of Electroneurodiagnostic Technology. 46 (1): 39–48. doi:10.1080/1086508X.2006.11079556. PMID 16605171.
- ↑ Malow BA (november 2005). »Sleep and epilepsy«. Neurologic Clinics. 23 (4): 1127–1147. doi:10.1016/j.ncl.2005.07.002. PMID 16243619.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Tinuper P, Provini F, Bisulli F, Vignatelli L, Plazzi G, Vetrugno R, Montagna P, Lugaresi E (Avgust 2007). »Movement disorders in sleep: guidelines for differentiating epileptic from non-epileptic motor phenomena arising from sleep«. Sleep Medicine Reviews. 11 (4): 255–267. doi:10.1016/j.smrv.2007.01.001. PMID 17379548.
- ↑ Scheffer IE, Berkovic S, Capovilla G, Connolly MB, French J, Guilhoto L, Hirsch E, Jain S, Mathern GW, Moshé SL, Nordli DR, Perucca E, Tomson T, Wiebe S, Zhang YH, Zuberi SM (april 2017). »ILAE classification of the epilepsies: Position paper of the ILAE Commission for Classification and Terminology«. Epilepsia. 58 (4): 512–521. doi:10.1111/epi.13709. PMC 5386840. PMID 28276062.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Mitchell WG (1996). »Status epilepticus and acute repetitive seizures in children, adolescents, and young adults: etiology, outcome, and treatment«. Epilepsia. 37 (s1): S74–S80. doi:10.1111/j.1528-1157.1996.tb06025.x. PMID 8647055.
- ↑ 42,0 42,1 Jafarpour S, Hirsch LJ, Gaínza-Lein M, Kellinghaus C, Detyniecki K (Maj 2019). »Seizure cluster: Definition, prevalence, consequences, and management«. Seizure. 68: 9–15. doi:10.1016/j.seizure.2018.05.013. PMID 29871784.
- ↑ Faught E (september 2022). »Economic aspects of treating seizure clusters«. Epilepsia. 63 (Suppl 1): S45–S54. doi:10.1111/epi.17340. PMID 35999172.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Haut SR, Shinnar S, Moshé SL (Januar 2005). »Seizure clustering: risks and outcomes«. Epilepsia. 46 (1): 146–149. doi:10.1111/j.0013-9580.2005.29004.x. PMID 15660781.
- ↑ Chen B, Choi H, Hirsch LJ, Katz A, Legge A, Wong RA, Jiang A, Kato K, Buchsbaum R, Detyniecki K (Julij 2017). »Prevalence and risk factors of seizure clusters in adult patients with epilepsy«. Epilepsy Research. 133: 98–102. doi:10.1016/j.eplepsyres.2017.04.016. PMID 28475999.
- ↑ Komaragiri A, Detyniecki K, Hirsch LJ (Junij 2016). »Seizure clusters: A common, understudied and undertreated phenomenon in refractory epilepsy«. Epilepsy & Behavior. 59: 83–86. doi:10.1016/j.yebeh.2016.02.030. PMID 27116535.
- ↑ Chung S, Szaflarski JP, Choi EJ, Wilson JC, Kharawala S, Kaur G, Hirsch LJ (november 2021). »A systematic review of seizure clusters: Prevalence, risk factors, burden of disease and treatment patterns«. Epilepsy Research. 177: 106748. doi:10.1016/j.eplepsyres.2021.106748. PMID 34521043.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Gidal B, Detyniecki K (september 2022). »Rescue therapies for seizure clusters: Pharmacology and target of treatments«. Epilepsia. 63 (Suppl 1): S34–S44. doi:10.1111/epi.17341. PMC 9543841. PMID 35999174.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Holmes, Thomas R. (2008). Handbook ofilepsy (4. izd.). Philadelphia: Lippincott Williams & Wilkins. str. 34. ISBN 978-0-7817-7397-3.
- ↑ 50,0 50,1 50,2 Panayiotopoulos, CP (2010). A clinical guide to epileptic syndromes and their treatment based on the ILAE classifications and practice parameter guidelines (Rev. 2. izd.). [London]: Springer. str. 445. ISBN 978-1-84628-644-5.
- ↑ James W. Wheless, ur. (2009). Advanced therapy in epilepsy. Shelton, Conn.: People's Medical Pub. House. str. 443. ISBN 978-1-60795-004-2.
- ↑ Larner, Andrew J. (2010). A dictionary of neurological signs (3. izd.). New York: Springer. str. 348. ISBN 978-1-4419-7095-4.
- ↑ Kaplan PW (november 2011). »Obsessive-compulsive disorder in chronic epilepsy«. Epilepsy & Behavior. 22 (3): 428–432. doi:10.1016/j.yebeh.2011.07.029. PMID 21889913.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Stefan H (2012). Epilepsy Part I: Basic Principles and Diagnosis E-Book: Handbook of Clinical Neurology (Volume 107 of Handbook of Clinical Neurology izd.). Newnes. str. 471. ISBN 978-0-444-53505-4.
- ↑ Plioplys S, Dunn DW, Caplan R (november 2007). »10-year research update review: psychiatric problems in children with epilepsy«. Journal of the American Academy of Child and Adolescent Psychiatry. 46 (11): 1389–1402. doi:10.1097/chi.0b013e31815597fc. PMID 18049289.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Reilly CJ (Maj–junij 2011). »Attention deficit hyperactivity disorder (ADHD) in childhood epilepsy«. Research in Developmental Disabilities. 32 (3): 883–893. doi:10.1016/j.ridd.2011.01.019. PMID 21310586.
- ↑ Levisohn PM (2007). »The autism-epilepsy connection«. Epilepsia. 48 (Suppl 9): 33–35. doi:10.1111/j.1528-1167.2007.01399.x. PMID 18047599.
- ↑ Lin JJ, Mula M, Hermann BP (september 2012). »Uncovering the neurobehavioural comorbidities of epilepsy over the lifespan«. Lancet. 380 (9848): 1180–1192. doi:10.1016/s0140-6736(12)61455-x. PMC 3838617. PMID 23021287.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Kanner AM, Schachter SC, Barry JJ, Hesdorffer DC, Mula M, Trimble M, Hermann B, Ettinger AE, Dunn D, Caplan R, Ryvlin P, Gilliam F, LaFrance WC (Junij 2012). »Depression and epilepsy: epidemiologic and neurobiologic perspectives that may explain their high comorbid occurrence«. Epilepsy & Behavior. 24 (2): 156–168. doi:10.1016/j.yebeh.2012.01.007. PMID 22632406.
- ↑ Adelöw C, Andersson T, Ahlbom A, Tomson T (Februar 2012). »Hospitalization for psychiatric disorders before and after onset of unprovoked seizures/epilepsy«. Neurology. 78 (6): 396–401. doi:10.1212/wnl.0b013e318245f461. PMID 22282649.
- ↑ Taylor RS, Sander JW, Taylor RJ, Baker GA (december 2011). »Predictors of health-related quality of life and costs in adults with epilepsy: a systematic review«. Epilepsia. 52 (12): 2168–2180. doi:10.1111/j.1528-1167.2011.03213.x. PMID 21883177.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Lacey CJ, Salzberg MR, Roberts H, Trauer T, D'Souza WJ (Avgust 2009). »Psychiatric comorbidity and impact on health service utilization in a community sample of patients with epilepsy«. Epilepsia. 50 (8): 1991–1994. doi:10.1111/j.1528-1167.2009.02165.x. PMID 19490049.
- ↑ Nogueira MH, Yasuda CL, Coan AC, Kanner AM, Cendes F (Julij 2017). »Concurrent mood and anxiety disorders are associated with pharmacoresistant seizures in patients with MTLE«. Epilepsia. 58 (7): 1268–1276. doi:10.1111/epi.13781. PMID 28555776.
- ↑ Kanner AM, Byrne R, Chicharro A, Wuu J, Frey M (Marec 2009). »A lifetime psychiatric history predicts a worse seizure outcome following temporal lobectomy«. Neurology. 72 (9): 793–799. doi:10.1212/01.wnl.0000343850.85763.9c. PMID 19255406.
- ↑ Boylan LS, Flint LA, Labovitz DL, Jackson SC, Starner K, Devinsky O (Januar 2004). »Depression but not seizure frequency predicts quality of life in treatment-resistant epilepsy«. Neurology. 62 (2): 258–261. doi:10.1212/01.wnl.0000103282.62353.85. PMID 14745064.
- ↑ Munger Clary HM, Croxton RD, Allan J, Lovato J, Brenes G, Snively BM, Wan M, Kimball J, Wong MH, O'Donovan CA, Conner K, Jones V, Duncan P (Marec 2020). »Who is willing to participate in research? A screening model for an anxiety and depression trial in the epilepsy clinic«. Epilepsy & Behavior. 104 (Pt A): 106907. doi:10.1016/j.yebeh.2020.106907. PMC 7282472. PMID 32000099.
- ↑ 67,0 67,1 67,2 Berkovic SF, Mulley JC, Scheffer IE, Petrou S (Julij 2006). »Human epilepsies: interaction of genetic and acquired factors«. Trends in Neurosciences. 29 (7): 391–397. doi:10.1016/j.tins.2006.05.009. PMID 16769131.
- ↑ Balestrini S, Arzimanoglou A, Blümcke I, Scheffer IE, Wiebe S, Zelano J, Walker MC (Februar 2021). »The aetiologies of epilepsy«. Epileptic Disorders. 23 (1): 1–16. doi:10.1684/epd.2021.1255. hdl:2158/1262349. PMID 33720020.
- ↑ 69,0 69,1 69,2 69,3 69,4 69,5 69,6 Neligan A, Hauser WA, Sander JW (2012). »The epidemiology of the epilepsies«. Epilepsy. Handbook of Clinical Neurology. Zv. 107. str. 113–33. doi:10.1016/B978-0-444-52898-8.00006-9. ISBN 978-0-444-52898-8. PMID 22938966.
- ↑ Steinlein OK (31. marec 2008). »Genetics and epilepsy«. Dialogues in Clinical Neuroscience. 10 (1): 29–38. doi:10.31887/DCNS.2008.10.1/oksteinlein. PMC 3181863. PMID 18472482.
- ↑ Dhavendra Kumar, ur. (2008). Genomics and clinical medicine. Oxford: Oxford University Press. str. 279. ISBN 978-0-19-972005-7. Arhivirano iz spletišča dne 21. maja 2016.
- ↑ 72,00 72,01 72,02 72,03 72,04 72,05 72,06 72,07 72,08 72,09 72,10 72,11 72,12 72,13 72,14 Bhalla D, Godet B, Druet-Cabanac M, Preux PM (Junij 2011). »Etiologies of epilepsy: a comprehensive review«. Expert Review of Neurotherapeutics. 11 (6): 861–876. doi:10.1586/ern.11.51. PMID 21651333.
- ↑ 73,0 73,1 Stafstrom CE, Staedtke V, Comi AM (2017). »Epilepsy Mechanisms in Neurocutaneous Disorders: Tuberous Sclerosis Complex, Neurofibromatosis Type 1, and Sturge-Weber Syndrome«. Frontiers in Neurology. 8: 87. doi:10.3389/fneur.2017.00087. PMC 5355446. PMID 28367137.
- ↑ O'Callaghan FJ, Shiell AW, Osborne JP, Martyn CN (Maj 1998). »Prevalence of tuberous sclerosis estimated by capture-recapture analysis«. Lancet. 351 (9114): 1490. doi:10.1016/S0140-6736(05)78872-3. PMID 9605811.
- ↑ 75,0 75,1 Northrup H, Aronow ME, Bebin EM, Bissler J, Darling TN, de Vries PJ, Frost MD, Fuchs Z, Gosnell ES, Gupta N, Jansen AC, Jóźwiak S, Kingswood JC, Knilans TK, McCormack FX, Pounders A, Roberds SL, Rodriguez-Buritica DF, Roth J, Sampson JR, Sparagana S, Thiele EA, Weiner HL, Wheless JW, Towbin AJ, Krueger DA (Oktober 2021). »Updated International Tuberous Sclerosis Complex Diagnostic Criteria and Surveillance and Management Recommendations«. Pediatric Neurology. 123: 50–66. doi:10.1016/j.pediatrneurol.2021.07.011. PMID 34399110.
- ↑ 76,0 76,1 Curatolo P (Marec 2015). »Mechanistic target of rapamycin (mTOR) in tuberous sclerosis complex-associated epilepsy«. Pediatric Neurology. 52 (3): 281–289. doi:10.1016/j.pediatrneurol.2014.10.028. PMID 25591831.
- ↑ Moavero R, Cerminara C, Curatolo P (november 2010). »Epilepsy secondary to tuberous sclerosis: lessons learned and current challenges«. Child's Nervous System. 26 (11): 1495–1504. doi:10.1007/s00381-010-1128-8. PMID 20358377.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Shirley MD, Tang H, Gallione CJ, Baugher JD, Frelin LP, Cohen B, North PE, Marchuk DA, Comi AM, Pevsner J (Maj 2013). »Sturge-Weber syndrome and port-wine stains caused by somatic mutation in GNAQ«. The New England Journal of Medicine. 368 (21): 1971–1979. doi:10.1056/NEJMoa1213507. PMC 3749068. PMID 23656586.
- ↑ 79,0 79,1 Sudarsanam A, Ardern-Holmes SL (Maj 2014). »Sturge-Weber syndrome: from the past to the present«. European Journal of Paediatric Neurology. 18 (3): 257–266. doi:10.1016/j.ejpn.2013.10.003. PMID 24275166.
- ↑ Sugano H, Iimura Y, Igarashi A, Nakazawa M, Suzuki H, Mitsuhashi T, Nakajima M, Higo T, Ueda T, Nakanishi H, Niijima S, Karagiozov K, Arai H (april 2021). »Extent of Leptomeningeal Capillary Malformation is Associated With Severity of Epilepsy in Sturge-Weber Syndrome«. Pediatric Neurology. 117: 64–71. doi:10.1016/j.pediatrneurol.2020.12.012. PMID 33677229.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Wang S, Pan J, Zhao M, Wang X, Zhang C, Li T, Wang M, Wang J, Zhou J, Liu C, Sun Y, Zhu M, Qi X, Luan G, Guan Y (Oktober 2022). »Characteristics, surgical outcomes, and influential factors of epilepsy in Sturge-Weber syndrome«. Brain. 145 (10): 3431–3443. doi:10.1093/brain/awab470. PMID 34932802.
- ↑ Lammert M, Friedman JM, Kluwe L, Mautner VF (Januar 2005). »Prevalence of neurofibromatosis 1 in German children at elementary school enrollment«. Archives of Dermatology. 141 (1): 71–74. doi:10.1001/archderm.141.1.71. PMID 15655144.
- ↑ Ostendorf AP, Gutmann DH, Weisenberg JL (Oktober 2013). »Epilepsy in individuals with neurofibromatosis type 1«. Epilepsia. 54 (10): 1810–1814. doi:10.1111/epi.12348. PMID 24032542.
- ↑ Barba C, Jacques T, Kahane P, Polster T, Isnard J, Leijten FS, Ozkara C, Tassi L, Giordano F, Castagna M, John A, Oz B, Salon C, Streichenberger N, Cross JH, Guerrini R (Avgust 2013). »Epilepsy surgery in Neurofibromatosis Type 1«. Epilepsy Research. 105 (3): 384–395. doi:10.1016/j.eplepsyres.2013.02.021. PMID 23597854.
- ↑ Galovic M, Döhler N, Erdélyi-Canavese B, Felbecker A, Siebel P, Conrad J, Evers S, Winklehner M, von Oertzen TJ, Haring HP, Serafini A, Gregoraci G, Valente M, Janes F, Gigli GL, Keezer MR, Duncan JS, Sander JW, Koepp MJ, Tettenborn B (Februar 2018). »Prediction of late seizures after ischaemic stroke with a novel prognostic model (the SeLECT score): a multivariable prediction model development and validation study«. The Lancet. Neurology. 17 (2): 143–152. doi:10.1016/S1474-4422(17)30404-0. PMID 29413315.
- ↑ Ren Z, Wen Q, Yan X, Wang Y, Zhang Y (september 2022). »Post-stroke epilepsy and risk of all-cause mortality: A systematic review and meta-analysis of cohort studies«. Clinical Neurology and Neurosurgery. 220: 107362. doi:10.1016/j.clineuro.2022.107362. PMID 35839716.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Zelano J, Holtkamp M, Agarwal N, Lattanzi S, Trinka E, Brigo F (Junij 2020). »How to diagnose and treat post-stroke seizures and epilepsy«. Epileptic Disorders. 22 (3): 252–263. doi:10.1684/epd.2020.1159. PMID 32597766.
- ↑ Zöllner JP, Schmitt FC, Rosenow F, Kohlhase K, Seiler A, Strzelczyk A, Stefan H (december 2021). »Seizures and epilepsy in patients with ischaemic stroke«. Neurological Research and Practice. 3 (1): 63. doi:10.1186/s42466-021-00161-w. PMC 8647498. PMID 34865660.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Grossman G (april 2008). »Neurological complications of coeliac disease: what is the evidence?«. Practical Neurology. 8 (2): 77–89. doi:10.1136/jnnp.2007.139717. PMID 18344378.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 90,0 90,1 90,2 Jackson JR, Eaton WW, Cascella NG, Fasano A, Kelly DL (Marec 2012). »Neurologic and psychiatric manifestations of celiac disease and gluten sensitivity«. The Psychiatric Quarterly. 83 (1): 91–102. doi:10.1007/s11126-011-9186-y. PMC 3641836. PMID 21877216.
- ↑ Shorvon SD (2011). The Causes of Epilepsy: Common and Uncommon Causes in Adults and Children. Cambridge University Press. str. 467. ISBN 978-1-139-49578-3.
- ↑ Sellner J, Trinka E (Oktober 2012). »Seizures and epilepsy in herpes simplex virus encephalitis: current concepts and future directions of pathogenesis and management«. Journal of Neurology. 259 (10): 2019–2030. doi:10.1007/s00415-012-6494-6. PMID 22527234.
- ↑ Hadjipanayis A, Hadjichristodoulou C, Youroukos S (Oktober 1997). »Epilepsy in patients with cerebral palsy«. Developmental Medicine and Child Neurology. 39 (10): 659–663. doi:10.1111/j.1469-8749.1997.tb07359.x. PMID 9352726.
- ↑ 94,0 94,1 Bromfield EB (2006). »Basic Mechanisms Underlying Seizures and Epilepsy«. An Introduction to Epilepsy. American Epilepsy Society.
- ↑ Blumenfeld H (2005). »Cellular and network mechanisms of spike-wave seizures«. Epilepsia. 46 (Suppl.9): 21–33. doi:10.1111/j.1528-1167.2005.00311.x. PMID 16302873.
- ↑ Noebels JL, Avoli M (29. junij 2012). Jasper's Basic Mechanisms of the Epilepsies. Oxford University Press. str. 466, 470. ISBN 978-0-19-974654-5. Pridobljeno 16. oktobra 2014.
- ↑ 97,0 97,1 Le Van Quyen M, Navarro V, Martinerie J, Baulac M, Varela FJ (2003). »Toward a neurodynamical understanding of ictogenesis«. Epilepsia. 44 (Suppl.12): 30–43. doi:10.1111/j.0013-9580.2003.12007.x. PMID 14641559.
- ↑ Lopes da Silva F, Blanes W, Kalitzin SN, Parra J, Suffczynski P, Velis DN (2003). »Epilepsies as dynamical diseases of brain systems: basic models of the transition between normal and epileptic activity«. Epilepsia. 44 (Suppl.12): 72–83. doi:10.1111/j.0013-9580.2003.12005.x. PMID 14641563.
- ↑ Henshall DC, Hamer HM, Pasterkamp RJ, Goldstein DB, Kjems J, Prehn JH, Schorge S, Lamottke K, Rosenow F (december 2016). »MicroRNAs in epilepsy: pathophysiology and clinical utility«. The Lancet. Neurology. 15 (13): 1368–1376. doi:10.1016/S1474-4422(16)30246-0. PMID 27839653.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Henshall DC (april 2014). »MicroRNA and epilepsy: profiling, functions and potential clinical applications«. Current Opinion in Neurology. 27 (2): 199–205. doi:10.1097/WCO.0000000000000079. PMC 4127484. PMID 24553459.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Oby E, Janigro D (november 2006). »The blood-brain barrier and epilepsy«. Epilepsia. 47 (11): 1761–1774. doi:10.1111/j.1528-1167.2006.00817.x. PMID 17116015.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Somjen GG (2004). Ions in the Brain Normal Function, Seizures, and Stroke. New York: Oxford University Press. str. 167. ISBN 978-0-19-803459-9.
- ↑ 103,0 103,1 Engel J, Pedley TA, ur. (2008). Epilepsy: a comprehensive textbook (2nd izd.). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. str. 483. ISBN 978-0-7817-5777-5.
- ↑ 104,00 104,01 104,02 104,03 104,04 104,05 104,06 104,07 104,08 104,09 104,10 104,11 104,12 104,13 104,14 104,15 104,16 104,17 104,18 104,19 104,20 104,21 104,22 104,23 104,24 104,25 National Clinical Guideline Centre (Januar 2012). The Epilepsies: The diagnosis and management of the epilepsies in adults and children in primary and secondary care (PDF). National Institute for Health and Clinical Excellence. str. 57–83. Arhivirano (PDF) iz spletišča dne 16. decembra 2013.
- ↑ Fisher RS, van Emde Boas W, Blume W, Elger C, Genton P, Lee P, Engel J (april 2005). »Epileptic seizures and epilepsy: definitions proposed by the International League Against Epilepsy (ILAE) and the International Bureau for Epilepsy (IBE)«. Epilepsia. 46 (4): 470–472. doi:10.1111/j.0013-9580.2005.66104.x. PMID 15816939.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Panayiotopoulos CP (december 2011). »The new ILAE report on terminology and concepts for organization of epileptic seizures: a clinician's critical view and contribution«. Epilepsia. 52 (12): 2155–2160. doi:10.1111/j.1528-1167.2011.03288.x. PMID 22004554.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 107,0 107,1 107,2 107,3 Ingrid E. Scheffer; Samuel Berkovic; Giuseppe Capovilla; Mary B. Connolly; Jacqueline French; Laura Guilhoto; Edouard Hirsch; Satish Jain; Gary W. Mathern; Solomon L. Moshé; Douglas R. Nordli; Emilio Perucca; Torbjörn Tomson; Samuel Wiebe; Yue-Hua Zhang; Sameer M. Zuberi (2017). »ILAE classification of the epilepsies: Position paper of the ILAE Commission for Classification and Terminology« (PDF). Epilepsia. 58 (4): 512–521. doi:10.1111/epi.13709.
- ↑ »Operational Classification of Seizure Types (2017)«. Arhivirano iz spletišča dne 9. aprila 2023.
- ↑ »Proposal for revised classification of epilepsies and epileptic syndromes. Commission on Classification and Terminology of the International League Against Epilepsy«. Epilepsia. 30 (4): 389–399. 1989. doi:10.1111/j.1528-1157.1989.tb05316.x. PMID 2502382.
- ↑ Engel J (Avgust 2006). »ILAE classification of epilepsy syndromes«. Epilepsy Research. 70 (Suppl 1): S5-10. doi:10.1016/j.eplepsyres.2005.11.014. PMID 16822650.
- ↑ Berg AT, Berkovic SF, Brodie MJ, Buchhalter J, Cross JH, van Emde Boas W, Engel J, French J, Glauser TA, Mathern GW, Moshé SL, Nordli D, Plouin P, Scheffer IE (april 2010). »Revised terminology and concepts for organization of seizures and epilepsies: report of the ILAE Commission on Classification and Terminology, 2005-2009«. Epilepsia. 51 (4): 676–685. doi:10.1111/j.1528-1167.2010.02522.x. PMID 20196795.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 112,0 112,1 112,2 112,3 112,4 112,5 Shorvon SD (Junij 2011). »The etiologic classification of epilepsy«. Epilepsia. 52 (6): 1052–1057. doi:10.1111/j.1528-1167.2011.03041.x. PMID 21449936.
- ↑ »Epilepsy syndromes«. International league against epilepsy. Arhivirano iz spletišča dne 6. oktobra 2014. Pridobljeno 6. oktobra 2014.
- ↑ Asadi-Pooya AA (Marec 2018). »Lennox-Gastaut syndrome: a comprehensive review«. Neurological Sciences. 39 (3): 403–414. doi:10.1007/s10072-017-3188-y. PMID 29124439.
- ↑ Chemaly N, Nabbout R. »Dravet Syndrome«.
- ↑ Chipaux M. »West syndrome«.
- ↑ Nordli DR (Oktober 2012). »Epileptic encephalopathies in infants and children«. Journal of Clinical Neurophysiology. 29 (5): 420–424. doi:10.1097/WNP.0b013e31826bd961. PMID 23027099.
- ↑ Heinzen EL, Depondt C, Cavalleri GL, Ruzzo EK, Walley NM, Need AC, Ge D, He M, Cirulli ET, Zhao Q, Cronin KD, Gumbs CE, Campbell CR, Hong LK, Maia JM, Shianna KV, McCormack M, Radtke RA, O'Conner GD, Mikati MA, Gallentine WB, Husain AM, Sinha SR, Chinthapalli K, Puranam RS, McNamara JO, Ottman R, Sisodiya SM, Delanty N, Goldstein DB (Avgust 2012). »Exome sequencing followed by large-scale genotyping fails to identify single rare variants of large effect in idiopathic generalized epilepsy«. American Journal of Human Genetics. 91 (2): 293–302. doi:10.1016/j.ajhg.2012.06.016. PMC 3415540. PMID 22863189.
- ↑ Carvill GL, Heavin SB, Yendle SC, McMahon JM, O'Roak BJ, Cook J, Khan A, Dorschner MO, Weaver M, Calvert S, Malone S, Wallace G, Stanley T, Bye AM, Bleasel A, Howell KB, Kivity S, Mackay MT, Rodriguez-Casero V, Webster R, Korczyn A, Afawi Z, Zelnick N, Lerman-Sagie T, Lev D, Møller RS, Gill D, Andrade DM, Freeman JL, Sadleir LG, Shendure J, Berkovic SF, Scheffer IE, Mefford HC (Julij 2013). »Targeted resequencing in epileptic encephalopathies identifies de novo mutations in CHD2 and SYNGAP1«. Nature Genetics. 45 (7): 825–830. doi:10.1038/ng.2646. PMC 3704157. PMID 23708187.
- ↑ Chénier S, Yoon G, Argiropoulos B, Lauzon J, Laframboise R, Ahn JW, Ogilvie CM, Lionel AC, Marshall CR, Vaags AK, Hashemi B, Boisvert K, Mathonnet G, Tihy F, So J, Scherer SW, Lemyre E, Stavropoulos DJ (2014). »CHD2 haploinsufficiency is associated with developmental delay, intellectual disability, epilepsy and neurobehavioural problems«. Journal of Neurodevelopmental Disorders. 6 (1): 9. doi:10.1186/1866-1955-6-9. PMC 4022362. PMID 24834135.
- ↑ Suls A, Jaehn JA, Kecskés A, Weber Y, Weckhuysen S, Craiu DC, Siekierska A, Djémié T, Afrikanova T, Gormley P, von Spiczak S, Kluger G, Iliescu CM, Talvik T, Talvik I, Meral C, Caglayan HS, Giraldez BG, Serratosa J, Lemke JR, Hoffman-Zacharska D, Szczepanik E, Barisic N, Komarek V, Hjalgrim H, Møller RS, Linnankivi T, Dimova P, Striano P, Zara F, Marini C, Guerrini R, Depienne C, Baulac S, Kuhlenbäumer G, Crawford AD, Lehesjoki AE, de Witte PA, Palotie A, Lerche H, Esguerra CV, De Jonghe P, Helbig I (november 2013). »De novo loss-of-function mutations in CHD2 cause a fever-sensitive myoclonic epileptic encephalopathy sharing features with Dravet syndrome«. American Journal of Human Genetics. 93 (5): 967–975. doi:10.1016/j.ajhg.2013.09.017. PMC 3824114. PMID 24207121.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ EuroEPINOMICS-RES Consortium (Oktober 2014). »De novo mutations in synaptic transmission genes including DNM1 cause epileptic encephalopathies«. American Journal of Human Genetics. 95 (4): 360–370. doi:10.1016/j.ajhg.2014.08.013. PMC 4185114. PMID 25262651.
- ↑ 123,0 123,1 »1 Guidance | Epilepsies: Diagnosis and management | Guidance | NICE«. 11. januar 2012.
- ↑ »American Epilepsy Society Choosing Wisely«. www.choosingwisely.org. 14. avgust 2018. Pridobljeno 30. avgusta 2018.
- ↑ Wallace SJ, Farrell K, ur. (2004). Epilepsy in children (2nd izd.). London: Arnold. str. 354. ISBN 978-0-340-80814-6.
- ↑ Chen WL, Mefford HC (Julij 2021). »Diagnostic Considerations in the Epilepsies-Testing Strategies, Test Type Advantages, and Limitations«. Neurotherapeutics. 18 (3): 1468–1477. doi:10.1007/s13311-021-01121-7. PMC 8608977. PMID 34532824.
- ↑ Aledo-Serrano A, Sánchez-Alcudia R, Toledano R, García-Morales I, Beltrán-Corbellini Á, del Pino I, Gil-Nagel A (2021). »Developmental and epileptic encephalopathies after negative or inconclusive genetic testing: what is next?«. Journal of Translational Genetics and Genomics. 5 (4): 443–455. doi:10.20517/jtgg.2021.40.
- ↑ Luef G (Oktober 2010). »Hormonal alterations following seizures«. Epilepsy & Behavior. 19 (2): 131–133. doi:10.1016/j.yebeh.2010.06.026. PMID 20696621.
- ↑ 129,0 129,1 Ahmad S, Beckett MW (Marec 2004). »Value of serum prolactin in the management of syncope«. Emergency Medicine Journal. 21 (2): 3e–3. doi:10.1136/emj.2003.008870. PMC 1726305. PMID 14988379.
- ↑ Shukla G, Bhatia M, Vivekanandhan S, Gupta N, Tripathi M, Srivastava A, Pandey RM, Jain S (Avgust 2004). »Serum prolactin levels for differentiation of nonepileptic versus true seizures: limited utility«. Epilepsy & Behavior. 5 (4): 517–521. doi:10.1016/j.yebeh.2004.03.004. PMID 15256189.
- ↑ Chen DK, So YT, Fisher RS (september 2005). »Use of serum prolactin in diagnosing epileptic seizures: report of the Therapeutics and Technology Assessment Subcommittee of the American Academy of Neurology«. Neurology. 65 (5): 668–675. doi:10.1212/01.wnl.0000178391.96957.d0. PMID 16157897.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Brodtkorb E (2013). »Common imitators of epilepsy«. Acta Neurologica Scandinavica. Supplementum. 127 (196): 5–10. doi:10.1111/ane.12043. PMID 23190285.
- ↑ 133,0 133,1 133,2 133,3 Marx JA, ur. (2010). Rosen's emergency medicine: concepts and clinical practice (7th izd.). Philadelphia: Mosby/Elsevier. str. 2228. ISBN 978-0-323-05472-0.
- ↑ 134,0 134,1 Zaidi A, Clough P, Cooper P, Scheepers B, Fitzpatrick AP (Julij 2000). »Misdiagnosis of epilepsy: many seizure-like attacks have a cardiovascular cause«. Journal of the American College of Cardiology. 36 (1): 181–184. doi:10.1016/S0735-1097(00)00700-2. PMID 10898432.
- ↑ Bisulli F, Vignatelli L, Provini F, Leta C, Lugaresi E, Tinuper P (december 2011). »Parasomnias and nocturnal frontal lobe epilepsy (NFLE): lights and shadows--controversial points in the differential diagnosis«. Sleep Medicine. 12 (Suppl 2): S27–S32. doi:10.1016/j.sleep.2011.10.008. PMID 22136895.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Zhou JQ, Zhou LM, Fang ZY, Wang Q, Chen ZY, Yang LB, Chen SD, Cai XD (Januar 2011). »Analyzing clinical and electrophysiological characteristics of Paroxysmal Dyskinesia«. Journal of Research in Medical Sciences. 16 (1): 110–114. PMC 3063430. PMID 21448393.
- ↑ Akhtar MJ (Marec 2002). »All seizures are not epilepsy: many have a cardiovascular cause«. JPMA. The Journal of the Pakistan Medical Association. 52 (3): 116–120. PMID 12071066.
- ↑ 138,0 138,1 Jerome E (2013). Seizures and epilepsy (2nd izd.). New York: Oxford University Press. str. 462. ISBN 978-0-19-532854-7.
- ↑ Helmers SL, Kobau R, Sajatovic M, Jobst BC, Privitera M, Devinsky O, Labiner D, Escoffery C, Begley CE, Shegog R, Pandey D, Fraser RT, Johnson EK, Thompson NJ, Horvath KJ (Marec 2017). »Self-management in epilepsy: Why and how you should incorporate self-management in your practice«. Epilepsy & Behavior. 68: 220–224. doi:10.1016/j.yebeh.2016.11.015. PMC 5381244. PMID 28202408.
- ↑ 140,0 140,1 140,2 140,3 Michael, GE.; O'Connor, RE. (Februar 2011). »The diagnosis and management of seizures and status epilepticus in the prehospital setting«. Emerg Med Clin North Am. 29 (1): 29–39. doi:10.1016/j.emc.2010.08.003. PMID 21109100.
- ↑ James W. Wheless; James Willmore; Roger A. Brumback (2009). Advanced therapy in epilepsy. Shelton, Conn.: People's Medical Pub. House. str. 144. ISBN 9781607950042.
- ↑ 142,0 142,1 142,2 National Clinical Guideline Centre (Januar 2012). The Epilepsies: The diagnosis and management of the epilepsies in adults and children in primary and secondary care (PDF). National Institute for Health and Clinical Excellence. Arhivirano (PDF) iz spletišča dne 16. decembra 2013.
- ↑ Elaine Wyllie (2012). Wyllie's Treatment of Epilepsy: Principles and Practice. Lippincott Williams & Wilkins. str. 187. ISBN 978-1-4511-5348-4.
- ↑ Steven R. Flanagan; Herb Zaretsky; Alex Moroz,, ur. (2010). Medical aspects of disability; a handbook for the rehabilitation professional (4. izd.). New York: Springer. str. 182. ISBN 978-0-8261-2784-6.
{{navedi knjigo}}: Vzdrževanje CS1: dodatno ločilo (povezava) - ↑ Nolan, SJ; Marson, AG; Pulman, J; Tudur Smith, C (23. avgust 2013). »Phenytoin versus valproate monotherapy for partial onset seizures and generalised onset tonic-clonic seizures«. The Cochrane database of systematic reviews. 8: CD001769. doi:10.1002/14651858.CD001769.pub2. PMID 23970302.
- ↑ Tudur Smith, C; Marson, AG; Clough, HE; Williamson, PR (2002). »Carbamazepine versus phenytoin monotherapy for epilepsy«. The Cochrane database of systematic reviews (2): CD001911. doi:10.1002/14651858.CD001911. PMID 12076427.
- ↑ Powell, G; Saunders, M; Marson, AG (20. januar 2010). »Immediate-release versus controlled-release carbamazepine in the treatment of epilepsy«. The Cochrane database of systematic reviews (1): CD007124. doi:10.1002/14651858.CD007124.pub2. PMID 20091617.
- ↑ Nevitt SJ, Sudell M, Cividini S, Marson AG, Tudur Smith C (april 2022). »Antiepileptic drug monotherapy for epilepsy: a network meta-analysis of individual participant data«. The Cochrane Database of Systematic Reviews. 2022 (4): CD011412. doi:10.1002/14651858.CD011412.pub4. PMC 8974892. PMID 35363878.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Ilangaratne, NB; Mannakkara, NN; Bell, GS; Sander, JW (1. december 2012). »Phenobarbital: missing in action«. Bulletin of the World Health Organization. 90 (12): 871-871A. doi:10.2471/BLT.12.113183. PMID 23284189.
- ↑ Shorvon, Simon; Perucca, Emilio; Engel Jr, Jerome, ur. (2009). The treatment of epilepsy (3. izd.). Chichester, UK: Wiley-Blackwell. str. 587. ISBN 9781444316674.
- ↑ 151,0 151,1 151,2 151,3 151,4 151,5 Perucca, P; Gilliam, FG (september 2012). »Adverse effects of antiepileptic drugs«. Lancet neurology. 11 (9): 792–802. doi:10.1016/S1474-4422(12)70153-9. PMID 22832500.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 152,0 152,1 152,2 152,3 Bromley R, Adab N, Bluett-Duncan M, Clayton-Smith J, Christensen J, Edwards K, Greenhalgh J, Hill RA, Jackson CF, Khanom S, McGinty RN, Tudur Smith C, Pulman J, Marson AG (Avgust 2023). »Monotherapy treatment of epilepsy in pregnancy: congenital malformation outcomes in the child«. The Cochrane Database of Systematic Reviews. 2023 (8): CD010224. doi:10.1002/14651858.CD010224.pub3. PMC 10463554. PMID 37647086.
{{navedi časopis}}: Check|pmid=value (pomoč); Preveri|pmc=vrednost (pomoč) - ↑ 153,0 153,1 Kamyar, M.; Varner, M. (Junij 2013). »Epilepsy in pregnancy«. Clin Obstet Gynecol. 56 (2): 330–41. doi:10.1097/GRF.0b013e31828f2436. PMID 23563876.
- ↑ Lawrence S. Neinstein, ur. (2008). Adolescent health care : a practical guide (5. izd.). Philadelphia: Lippincott Williams & Wilkins. str. 335. ISBN 978-0-7817-9256-1.
- ↑ 155,0 155,1 Brodie MJ, Elder AT, Kwan P (november 2009). »Epilepsy in later life«. The Lancet. Neurology. 8 (11): 1019–1030. doi:10.1016/S1474-4422(09)70240-6. PMID 19800848.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Tsou, Amy Y.; Kessler, Sudha Kilaru; Wu, Mingche; Abend, Nicholas S.; Massey, Shavonne L.; Treadwell, Jonathan R. (3. januar 2023). »Surgical Treatments for Epilepsies in Children Aged 1–36 Months: A Systematic Review«. Neurology. 100 (1): e1–e15. doi:10.1212/WNL.0000000000201012. PMC 9827129. PMID 36270898.
- ↑ 157,0 157,1 Krucoff MO, Chan AY, Harward SC, Rahimpour S, Rolston JD, Muh C, Englot DJ (december 2017). »Rates and predictors of success and failure in repeat epilepsy surgery: A meta-analysis and systematic review«. Epilepsia. 58 (12): 2133–2142. doi:10.1111/epi.13920. PMC 5716856. PMID 28994113.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Benoit PW, Yagiela A, Fort NF (Februar 1980). »Pharmacologic correlation between local anesthetic-induced myotoxicity and disturbances of intracellular calcium distribution«. Toxicology and Applied Pharmacology. 52 (2): 187–198. Bibcode:1980ToxAP..52..187B. doi:10.1016/0041-008x(80)90105-2. PMID 7361318.
- ↑ 159,0 159,1 159,2 159,3 159,4 Duncan JS (april 2007). »Epilepsy surgery«. Clinical Medicine. 7 (2): 137–142. doi:10.7861/clinmedicine.7-2-137. PMC 4951827. PMID 17491501.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Birbeck GL, Hays RD, Cui X, Vickrey BG (Maj 2002). »Seizure reduction and quality of life improvements in people with epilepsy«. Epilepsia. 43 (5): 535–538. doi:10.1046/j.1528-1157.2002.32201.x. PMID 12027916.
- ↑ Edwards CA, Kouzani A, Lee KH, Ross EK (september 2017). »Neurostimulation Devices for the Treatment of Neurologic Disorders«. Mayo Clinic Proceedings. 92 (9): 1427–1444. doi:10.1016/j.mayocp.2017.05.005. PMID 28870357.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Panebianco M, Rigby A, Marson AG (Julij 2022). »Vagus nerve stimulation for focal seizures«. The Cochrane Database of Systematic Reviews. 2022 (7): CD002896. doi:10.1002/14651858.CD002896.pub3. PMC 9281624. PMID 35833911.
- ↑ Treadwell JR, Wu M, Tsou AY (2022). Management of Infantile Epilepsies: A Systematic Review (poročilo). doi:10.23970/AHRQEPCCER252. PMID 36383706.
- ↑ Maria BL, ur. (2009). Current management in child neurology (4th izd.). Hamilton, Ont.: BC Decker. str. 180. ISBN 978-1-60795-000-4. Arhivirano iz spletišča dne 24. junija 2016.
- ↑ Verrotti A, Tocco AM, Salladini C, Latini G, Chiarelli F (november 2005). »Human photosensitivity: from pathophysiology to treatment«. European Journal of Neurology. 12 (11): 828–841. doi:10.1111/j.1468-1331.2005.01085.x. PMID 16241971.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Tan G, Thornby J, Hammond DC, Strehl U, Canady B, Arnemann K, Kaiser DA (Julij 2009). »Meta-analysis of EEG biofeedback in treating epilepsy«. Clinical EEG and Neuroscience. 40 (3): 173–179. doi:10.1177/155005940904000310. PMID 19715180.
- ↑ Arida RM, Scorza FA, Scorza CA, Cavalheiro EA (Marec 2009). »Is physical activity beneficial for recovery in temporal lobe epilepsy? Evidences from animal studies«. Neuroscience and Biobehavioral Reviews. 33 (3): 422–431. doi:10.1016/j.neubiorev.2008.11.002. PMID 19059282.
- ↑ Arida RM, Cavalheiro EA, da Silva AC, Scorza FA (2008). »Physical activity and epilepsy: proven and predicted benefits«. Sports Medicine. 38 (7): 607–615. doi:10.2165/00007256-200838070-00006. PMID 18557661.
- ↑ Di Vito L, Naldi I, Mostacci B, Licchetta L, Bisulli F, Tinuper P (Junij 2010). »A seizure response dog: video recording of reacting behaviour during repetitive prolonged seizures«. Epileptic Disorders. 12 (2): 142–145. doi:10.1684/epd.2010.0313. PMID 20472528.
- ↑ Kirton A, Winter A, Wirrell E, Snead OC (Oktober 2008). »Seizure response dogs: evaluation of a formal training program«. Epilepsy & Behavior. 13 (3): 499–504. doi:10.1016/j.yebeh.2008.05.011. PMID 18595778.
- ↑ Doherty MJ, Haltiner AM (Januar 2007). »Wag the dog: skepticism on seizure alert canines«. Neurology. 68 (4): 309. doi:10.1212/01.wnl.0000252369.82956.a3. PMID 17242343.
- ↑ 172,0 172,1 172,2 Michaelis R, Tang V, Wagner JL, Modi AC, LaFrance WC, Goldstein LH, Lundgren T, Reuber M (Oktober 2017). »Psychological treatments for people with epilepsy«. The Cochrane Database of Systematic Reviews. 10 (10): CD012081. doi:10.1002/14651858.CD012081.pub2. PMC 6485515. PMID 29078005.
- ↑ Stockings E, Zagic D, Campbell G, Weier M, Hall WD, Nielsen S, Herkes GK, Farrell M, Degenhardt L (Julij 2018). »Evidence for cannabis and cannabinoids for epilepsy: a systematic review of controlled and observational evidence«. Journal of Neurology, Neurosurgery, and Psychiatry. 89 (7): 741–753. doi:10.1136/jnnp-2017-317168. hdl:1959.4/unsworks_50076. PMID 29511052.
- ↑ Cannabis derivative may reduce seizures in some severe drug-resistant epilepsies, but adverse events increase (poročilo). 26. junij 2018. doi:10.3310/signal-000606.
- ↑ »Press Announcements - FDA approves first drug comprised of an active ingredient derived from marijuana to treat rare, severe forms of epilepsy«. www.fda.gov (v angleščini). 25. junij 2018. Pridobljeno 4. oktobra 2018.
- ↑ »Archive of "Journal of Investigative Medicine High Impact Case Reports". – PMC«. www.ncbi.nlm.nih.gov.
- ↑ Cheuk DK, Wong V (Maj 2014). »Acupuncture for epilepsy«. The Cochrane Database of Systematic Reviews. 2014 (5): CD005062. doi:10.1002/14651858.CD005062.pub4. PMC 10105317. PMID 24801225.
{{navedi časopis}}: Preveri|pmc=vrednost (pomoč) - ↑ Ranganathan LN, Ramaratnam S (april 2005). »Vitamins for epilepsy«. The Cochrane Database of Systematic Reviews (2): CD004304. doi:10.1002/14651858.CD004304.pub2. PMID 15846704.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Panebianco M, Sridharan K, Ramaratnam S (Oktober 2017). »Yoga for epilepsy«. The Cochrane Database of Systematic Reviews. 2017 (10): CD001524. doi:10.1002/14651858.CD001524.pub3. PMC 6485327. PMID 28982217.
- ↑ 180,0 180,1 Brigo F, Igwe SC, Del Felice A (Avgust 2016). »Melatonin as add-on treatment for epilepsy«. The Cochrane Database of Systematic Reviews. 2016 (8): CD006967. doi:10.1002/14651858.CD006967.pub4. PMC 7386917. PMID 27513702.
- ↑ He LY, Hu MB, Li RL, Zhao R, Fan LH, He L, Lu F, Ye X, Huang YL, Wu CJ (2021). »Natural Medicines for the Treatment of Epilepsy: Bioactive Components, Pharmacology and Mechanism«. Frontiers in Pharmacology. 12: 604040. doi:10.3389/fphar.2021.604040. PMC 7969896. PMID 33746751.
- ↑ Aguiar CC, Almeida AB, Araújo PV, de Abreu RN, Chaves EM, do Vale OC, Macêdo DS, Woods DJ, Fonteles MM, Vasconcelos SM (2012). »Oxidative stress and epilepsy: literature review«. Oxidative Medicine and Cellular Longevity. 2012: 795259. doi:10.1155/2012/795259. PMC 3403512. PMID 22848783.
- ↑ 183,00 183,01 183,02 183,03 183,04 183,05 183,06 183,07 183,08 183,09 183,10 183,11 183,12 183,13 King A, Gerard EE (april 2022). »Contraception, fecundity, and pregnancy in women with epilepsy: an update on recent literature«. Current Opinion in Neurology. 35 (2): 161–168. doi:10.1097/WCO.0000000000001039. PMC 9230745. PMID 35191408.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 184,0 184,1 Reimers A, Brodtkorb E, Sabers A (Maj 2015). »Interactions between hormonal contraception and antiepileptic drugs: Clinical and mechanistic considerations«. Seizure. 28: 66–70. doi:10.1016/j.seizure.2015.03.006. PMID 25843765.
- ↑ »Enzyme-inducing antiepileptic drugs«. NICE. Maj 2023. Pridobljeno 2. novembra 2023.
- ↑ 186,0 186,1 186,2 Tomson T, Battino D, Bromley R, Kochen S, Meador K, Pennell P, Thomas SV (december 2019). »Management of epilepsy in pregnancy: a report from the International League Against Epilepsy Task Force on Women and Pregnancy«. Epileptic Disorders. 21 (6): 497–517. doi:10.1684/epd.2019.1105. hdl:11336/119061. PMID 31782407.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 187,0 187,1 Kwan, Patrick (2012). Fast facts : epilepsy (5. izd.). Abingdon, Oxford, UK: Health Press. str. 10. ISBN 1-908541-12-1.
- ↑ Fisher, Robert S.; Acevedo, Carlos; Arzimanoglou, Alexis; Bogacz, Alicia; Cross, J. Helen; Elger, Christian E.; Engel, Jerome; Forsgren, Lars; French, Jacqueline A.; Glynn, Mike; Hesdorffer, Dale C.; Lee, B.I.; Mathern, Gary W.; Moshé, Solomon L.; Perucca, Emilio (april 2014). »ILAE Official Report: A practical clinical definition of epilepsy«. Epilepsia. 55 (4): 475–482. doi:10.1111/epi.12550. PMID 24730690.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 189,0 189,1 189,2 Hitiris N, Mohanraj R, Norrie J, Brodie MJ (Maj 2007). »Mortality in epilepsy«. Epilepsy & Behavior. 10 (3): 363–376. doi:10.1016/j.yebeh.2007.01.005. PMID 17337248.
- ↑ 190,0 190,1 190,2 Shorvon S, Perucca E, Engel J, ur. (2009). The treatment of epilepsy (3rd izd.). Chichester, UK: Wiley-Blackwell. str. 28. ISBN 978-1-4443-1667-4. Arhivirano iz spletišča dne 10. junija 2016.
- ↑ 191,0 191,1 Bagary M (april 2011). »Epilepsy, antiepileptic drugs and suicidality«. Current Opinion in Neurology. 24 (2): 177–182. doi:10.1097/WCO.0b013e328344533e. PMID 21293270.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Mula M, Sander JW (Avgust 2013). »Suicide risk in people with epilepsy taking antiepileptic drugs«. Bipolar Disorders. 15 (5): 622–627. doi:10.1111/bdi.12091. PMID 23755740.
- ↑ 193,0 193,1 Ryvlin P, Nashef L, Tomson T (Maj 2013). »Prevention of sudden unexpected death in epilepsy: a realistic goal?«. Epilepsia. 54 (Suppl 2): 23–28. doi:10.1111/epi.12180. PMID 23646967.
- ↑ Kløvgaard M, Sabers A, Ryvlin P (november 2022). »Update on Sudden Unexpected Death in Epilepsy«. Neurologic Clinics. 40 (4): 741–754. doi:10.1016/j.ncl.2022.06.001. PMID 36270688.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Hirtz D; Thurman DJ; Gwinn-Hardy K; Mohamed M; Chaudhuri AR; Zalutsky R (30. januar 2007). »How common are the 'common' neurologic disorders?«. Neurology. 68 (5): 326–37. doi:10.1212/01.wnl.0000252807.38124.a3. PMID 17261678.
- ↑ Vos T, Allen C, Arora M, Barber RM, Bhutta ZA, Brown A, Carter A, Casey DC, Charlson FJ, Chen AZ, Coggeshall M, Cornaby L, Dandona L, Dicker DJ, Dilegge T, Erskine HE, Ferrari AJ, Fitzmaurice C, Fleming T, Forouzanfar MH, Fullman N, Gething PW, Goldberg EM, Graetz N, Haagsma JA, Hay SI, Johnson CO, Kassebaum NJ, Kawashima T, Kemmer L (Oktober 2016). »Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015«. Lancet. 388 (10053): 1545–1602. doi:10.1016/S0140-6736(16)31678-6. PMC 5055577. PMID 27733282.
- ↑ Espinosa-Jovel C, Toledano R, Aledo-Serrano Á, García-Morales I, Gil-Nagel A (Marec 2018). »Epidemiological profile of epilepsy in low income populations«. Seizure. 56: 67–72. doi:10.1016/j.seizure.2018.02.002. PMID 29453113.
- ↑ 198,0 198,1 Sander JW (2003). »The epidemiology of epilepsy revisited«. Current Opinion in Neurology. 16 (2): 165–70. doi:10.1097/00019052-200304000-00008. PMID 12644744.
- ↑ 199,0 199,1 199,2 199,3 199,4 199,5 199,6 199,7 Saraceno, B; Avanzini, G; Lee, P, ur. (2005). Atlas: Epilepsy Care in the World (PDF). World Health Organization. ISBN 92-4-156303-6. Pridobljeno 20. decembra 2013.
- ↑ Mervyn J. Eadie; Peter F. Bladin (2001). A Disease Once Sacred: A History of the Medical Understanding of Epilepsy. John Libbey Eurotext. ISBN 978-0-86196-607-3.
- ↑ »Epilepsy: An historical overview«. World Health Organization. Februar 2001. Pridobljeno 27. decembra 2013.
- ↑ 202,0 202,1 Temkin O (1. marec 1994). The Falling Sickness: A History of Epilepsy from the Greeks to the Beginnings of Modern Neurology (v angleščini). JHU Press. str. Section 1. ISBN 978-1-4214-0053-2.
- ↑ Stol M (1993). Epilepsy in Babylonia (v angleščini). BRILL. str. 143. ISBN 978-90-72371-63-8.
- ↑ Harding GF, Jeavons PM (1994). Photosensitive Epilepsy (v angleščini). Cambridge University Press. str. 2. ISBN 978-1-898683-02-5.
- ↑ 205,0 205,1 Jilek-Aall L (Marec 1999). »Morbus sacer in Africa: some religious aspects of epilepsy in traditional cultures«. Epilepsia. 40 (3): 382–386. doi:10.1111/j.1528-1157.1999.tb00723.x. PMID 10080524.
- ↑ »Epilepsy and its Management: A Review«. ResearchGate. Januar 2012. Pridobljeno 22. februarja 2022.
- ↑ Illes J (2011). Encyclopedia of Mystics, Saints & Sages. HarperCollins. str. 1238. ISBN 978-0-06-209854-2. Arhivirano iz spletišča dne 11. januarja 2014.
Saint Valentine is invoked for healing as well as love. He protects against fainting and is requested to heal epilepsy and other seizure disorders. In northern Italy, epilepsy was once traditionally known as Saint Valentine's Malady.
- ↑ 208,0 208,1 208,2 Lewis E (17. februar 2012). Report of The Trial and Conviction of John Haggerty, for The Murder of Melchoir Fordney, Late of The City of Lancaster, Pennsylvania. Gale, Making of Modern Law. str. 62. ISBN 978-1-275-31136-7.
- ↑ Caravati, E. Martin (2004). Medical toxicology (3. izd.). Philadelphia [u.a.]: Lippincott Williams & Wilkins. str. 789. ISBN 978-0-7817-2845-4.
- ↑ 210,0 210,1 de Boer HM (december 2010). »Epilepsy stigma: moving from a global problem to global solutions«. Seizure. 19 (10): 630–636. doi:10.1016/j.seizure.2010.10.017. PMID 21075013.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Erkal, Emre; Kiyak, Emine; Uren, Yavuz; Milanlioglu, Aysel (Oktober 2024). »Determination of stigma and attitude in relatives of patients with epilepsy«. Seizure: European Journal of Epilepsy. 121: 64–69. doi:10.1016/j.seizure.2024.07.022. PMID 39089140.
{{navedi časopis}}: Check|pmid=value (pomoč) - ↑ Martindale, JL; Goldstein, JN; Pallin, DJ (Februar 2011). »Emergency department seizure epidemiology«. Emergency medicine clinics of North America. 29 (1): 15–27. doi:10.1016/j.emc.2010.08.002. PMID 21109099.
- ↑ Pellinen J, Tafuro E, Yang A, Price D, Friedman D, Holmes M, Barnard S, Detyniecki K, Hegde M, Hixson J, Haut S, Kälviäinen R, French J (december 2020). »Focal nonmotor versus motor seizures: The impact on diagnostic delay in focal epilepsy«. Epilepsia. 61 (12): 2643–2652. doi:10.1111/epi.16707. PMID 33078409.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 214,0 214,1 214,2 Engel J, Pedley TA, ur. (2008). Epilepsy: a comprehensive textbook (2nd izd.). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. str. 2279. ISBN 978-0-7817-5777-5.
- ↑ »Priloga 1: Merila za ugotavljanje telesne in duševne zmožnosti za kandidate za voznike in voznike« (PDF). Uradni list Republike Slovenije. 11. februar 2022. Pridobljeno 30. januarja 2025.
- ↑ »Spremembe pri zdravstvenih pogojih za voznike z očesnimi okvarami in epilepsijo«. MMC RTV-SLO. 7. februar 2022.
- ↑ Bor R (2012). Aviation Mental Health: Psychological Implications for Air Transportation. Ashgate Publishing. str. 148. ISBN 978-1-4094-8491-2.
- ↑ 218,0 218,1 »Seizure Disorders«. Transport Canada. Government of Canada. Arhivirano iz prvotnega spletišča dne 30. decembra 2013. Pridobljeno 29. decembra 2013.
- ↑ Wilner AN (2008). Epilepsy 199 answers: a doctor responds to his patients' questions (3rd izd.). New York: Demos Health. str. 52. ISBN 978-1-934559-96-3. Arhivirano iz spletišča dne 17. maja 2016.
- ↑ »Guide for Aviation Medical Examiners«. Federal Aviation Administration. Arhivirano iz spletišča dne 17. oktobra 2013. Pridobljeno 29. decembra 2013.
- ↑ 221,0 221,1 »National PPL (NPPL) Medical Requirements«. Civil Aviation Authority. Arhivirano iz spletišča dne 16. oktobra 2013. Pridobljeno 29. decembra 2013.
- ↑ Drivers Medical Group (2013). »For Medical Practitioners: At a glance Guide to the current Medical Standards of Fitness to Drive« (PDF). str. 8. Arhivirano (PDF) iz spletišča dne 30. decembra 2013. Pridobljeno 29. decembra 2013.
- ↑ »Društvo«. Društvo Liga proti epilepsiji Slovenije. Pridobljeno 29. januarja 2025.
- ↑ Aleem MA (Februar 2015). »World epilepsy day«. Epilepsia. 56 (2): 168. doi:10.1111/epi.12814. PMID 25404065.
- ↑ Perucca E (Februar 2015). »Commentary: why an international epilepsy day?«. Epilepsia. 56 (2): 170–171. doi:10.1111/epi.12813. PMID 25403985.
- ↑ Carr F (26. marec 2018). »People Are Wearing Purple Today for Epilepsy Awareness Day. Here's What That Is«. Time. Pridobljeno 18. aprila 2018.
- ↑ 227,0 227,1 Carney PR, Myers S, Geyer JD (december 2011). »Seizure prediction: methods«. Epilepsy & Behavior. 22 (Suppl 1): S94-101. doi:10.1016/j.yebeh.2011.09.001. PMC 3233702. PMID 22078526.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Engel J, ur. (2008). Epilepsy: a comprehensive textbook (2nd izd.). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. str. 426. ISBN 978-0-7817-5777-5.
- ↑ Guillemain, I., Kahane, P. & Depaulis, A. Animal models to study aetiopathology of epilepsy: what are the features to model? Epileptic Disord 14, 217–225 (2012).
- ↑ Jarre, G., Guillemain, I., and, C. D. M. of S. & 2017. Genetic Models of Absence Epilepsy in Rats and Mice. Elsevier 455–471 (2017)
- ↑ Depaulis, A. & Charpier, S. Pathophysiology of absence epilepsy: Insights from genetic models. Neurosci Lett 667, 53–65 (2018)
- ↑ Morris G, Heiland M, Lamottke K, Guan H, Hill T, Zhou Y, Zhu Q, Schorge S, Henshall DC (Januar 2022). »BICS01 Mediates Reversible Anti-seizure Effects in Brain Slice Models of Epilepsy«. Frontiers in Neurology. 12: 791608. doi:10.3389/fneur.2021.791608. PMC 8770400. PMID 35069421.
- ↑ Jirsa, Viktor K.; Stacey, William C.; Quilichini, Pascale P.; Ivanov, Anton I.; Bernard, Christophe (Avgust 2014). »On the nature of seizure dynamics«. Brain (v angleščini). 137 (8): 2210–2230. doi:10.1093/brain/awu133. ISSN 1460-2156. PMC 4107736. PMID 24919973.
- ↑ Chizhov, Anton V.; Zefirov, Artyom V.; Amakhin, Dmitry V.; Smirnova, Elena Yu; Zaitsev, Aleksey V. (31. maj 2018). »Minimal model of interictal and ictal discharges "Epileptor-2"«. PLOS Computational Biology (v angleščini). 14 (5): e1006186. Bibcode:2018PLSCB..14E6186C. doi:10.1371/journal.pcbi.1006186. ISSN 1553-7358. PMC 6005638. PMID 29851959.
- ↑ »Epileptor-2 model«.
- ↑ Kegler A, Pascotini ET, Caprara AL, Arend J, Gabbi P, Duarte MM, Royes LF, Fighera MR (Februar 2021). »Relationship between seizure type, metabolic profile, and inflammatory markers in blood samples of patients with epilepsy«. Epileptic Disorders. 23 (1): 74–84. doi:10.1684/epd.2021.1236. PMID 33602662.
- ↑ Walker MC, Schorge S, Kullmann DM, Wykes RC, Heeroma JH, Mantoan L (september 2013). »Gene therapy in status epilepticus«. Epilepsia. 54 (Suppl 6): 43–45. doi:10.1111/epi.12275. PMID 24001071.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Panebianco M, Walker L, Marson AG, in sod. (Cochrane Epilepsy Group) (Oktober 2023). »Immunomodulatory interventions for focal epilepsy«. The Cochrane Database of Systematic Reviews. 2023 (10): CD009945. doi:10.1002/14651858.CD009945.pub3. PMC 10577807. PMID 37842826.
{{navedi časopis}}: Check|pmid=value (pomoč); Preveri|pmc=vrednost (pomoč) - ↑ Quigg M, Rolston J, Barbaro NM (Januar 2012). »Radiosurgery for epilepsy: clinical experience and potential antiepileptic mechanisms«. Epilepsia. 53 (1): 7–15. doi:10.1111/j.1528-1167.2011.03339.x. PMC 3519388. PMID 22191545.
- ↑ 240,0 240,1 Thomas, WB (Januar 2010). »Idiopathic epilepsy in dogs and cats«. Veterinary Clinics of North America, Small Animal Practice. 40 (1): 161–79. doi:10.1016/j.cvsm.2009.09.004. PMID 19942062.
- ↑ Rundfeldt C, Löscher W (Januar 2014). »The pharmacology of imepitoin: the first partial benzodiazepine receptor agonist developed for the treatment of epilepsy«. CNS Drugs. 28 (1): 29–43. doi:10.1007/s40263-013-0129-z. PMID 24357084.
- ↑ van der Ree, M; Wijnberg, I (2012). »A review on epilepsy in the horse and the potential of Ambulatory EEG as a diagnostic tool«. The Veterinary quarterly. 32 (3–4): 159–67. doi:10.1080/01652176.2012.744496. PMID 23163553.
- ↑ Ciosek, Julia; Kimes, Abigail; Vinardell, Tatiana; Miller, Donald C; Antczak, Douglas F; Brooks, Samantha (23. avgust 2023). »Juvenile idiopathic epilepsy in Arabian horses is not a single-gene disorder«. Journal of Heredity. 114 (5): 488–491. doi:10.1093/jhered/esad029. PMID 37145017.
Nadaljnje branje
[uredi | uredi kodo]- National Institute for Health and Clinical Excellence (Januar 2012). The Epilepsies: The diagnosis and management of the epilepsies in adults and children in primary and secondary care (PDF). National Clinical Guideline Centre.
- Saraceno, B; Avanzini, G; Lee, P, ur. (2005). Atlas: Epilepsy Care in the World (PDF). World Health Organization. ISBN 92-4-156303-6. Pridobljeno 20. decembra 2013.
